solo per uso di ricerca
Dovitinib (TKI258) Lactate monohydrate FLT3 inibitore
N. Cat.S7765
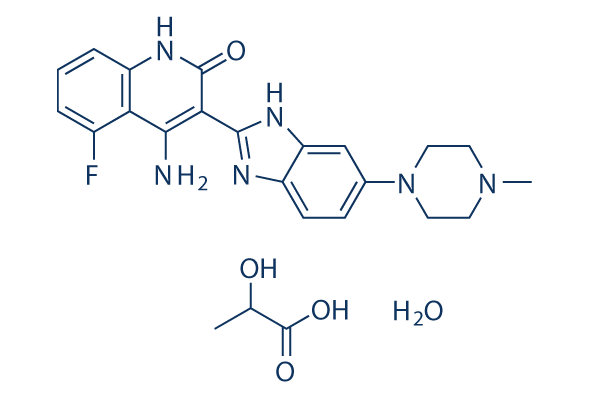
Struttura chimica
Peso molecolare: 500.52
Controllo Qualità
| Target correlati | EGFR VEGFR JAK PDGFR FGFR Src HIF FLT HER2 Bcr-Abl |
|---|---|
| Altro FLT3 Inibitori | UNC2025 Crenolanib (CP-868596) Dovitinib (TKI-258) Tandutinib (MLN518) KW-2449 ENMD-2076 AST-487 (NVP-AST487) TCS 359 G-749 AMG 925 |
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 500.52 | Formula | C24H29FN6O5 |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 915769-50-5 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
| Sinonimi | CHIR258 | Smiles | CC(C(=O)O)O.CN1CCN(CC1)C2=CC3=C(C=C2)N=C(N3)C4=C(C5=C(C=CC=C5F)NC4=O)N.O | ||
Solubilità
|
In vitro |
DMSO
: 100 mg/mL
(199.79 mM)
Water : 66 mg/mL Ethanol : 1 mg/mL |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Targets/IC50/Ki |
FLT3
1 nM
c-Kit
2 nM
FGFR1
8 nM
VEGFR3/FLT4
8 nM
FGFR3
9 nM
VEGFR1/FLT1
10 nM
VEGFR2/Flk1
13 nM
PDGFRβ
27 nM
CSF-1R/c-Fms
36 nM
|
|---|---|
| In vitro |
Dovitinib inibisce potentemente la crescita stimolata da FGF delle cellule B9 che esprimono WT e F384L-FGFR3 con un IC50 di 25 nM. Inoltre, Dovitinib inibisce la proliferazione delle cellule B9 che esprimono ciascuno dei vari mutanti attivati di FGFR3. È interessante notare che ci sono minime differenze osservate nella sensibilità delle diverse mutazioni di FGFR3 a Dovitinib, con l'IC50 che varia da 70 a 90 nM per ciascuna delle varie mutazioni. Le cellule B9 dipendenti da IL-6 contenenti solo il vettore (cellule B9-MINV) sono resistenti all'attività inibitoria di Dovitinib a concentrazioni fino a 1 μM. Dovitinib inibisce la proliferazione cellulare delle cellule KMS11 (FGFR3-Y373C), OPM2 (FGFR3-K650E) e KMS18 (FGFR3-G384D) con IC50 di 90 nM (KMS11 e OPM2) e 550 nM, rispettivamente. Dovitinib inibisce la fosforilazione di ERK1/2 mediata da FGF e induce citotossicità nelle cellule primarie di MM che esprimono FGFR3. Le BMSCs conferiscono un modesto grado di resistenza con il 44,6% di inibizione della crescita per le cellule trattate con 500 nM di Dovitinib e coltivate su stroma rispetto al 71,6% di inibizione della crescita per le cellule cresciute senza BMSCs. Dovitinib inibisce la proliferazione di M-NFS-60, una linea cellulare mieloblastica murina guidata dalla crescita di M-CSF con una concentrazione efficace mediana (EC50) di 220 nM. Il trattamento delle cellule SK-HEP1 con Dovitinib si traduce in una riduzione dose-dipendente del numero di cellule e un arresto in fase G2/M con riduzione delle fasi G0/G1 e S, inibizione della crescita indipendente dall'ancoraggio e blocco della motilità cellulare indotta da bFGF. L'IC50 per Dovitinib nelle cellule SK-HEP1 è di circa 1,7 μM. Dovitinib riduce anche significativamente i livelli di fosforilazione basale di FGFR-1, del substrato 2α di FGFR (FRS2-α) e di ERK1/2 ma non di Akt sia nelle cellule SK-HEP1 che nelle 21-0208. Nelle cellule HCC 21-0208, Dovitinib inibisce significativamente la fosforilazione indotta da bFGF di FGFR-1, FRS2-α, ERK1/2 ma non di Akt. |
| Saggio chinasico |
Saggi di chinasi in vitro
|
|
I valori della concentrazione inibitoria del 50% (IC50) per l'inibizione delle RTK da parte di Dovitinib sono determinati in un formato di fluorescenza risolta nel tempo (TRF) o radioattivo, misurando l'inibizione da parte di Dovitinib del trasferimento di fosfato a un substrato da parte del rispettivo enzima. I domini chinasi di FGFR3, FGFR1, PDGFRβ e VEGFR1-3 sono saggiati in 50 mM HEPES (acido N-2-idrossietilpiperazina-N'-2-etansolfonico), pH 7.0, 2 mM MgCl2, 10 mM MnCl2 1 mM NaF, 1 mM ditiotreitolo (DTT), 1 mg/mL di albumina sierica bovina (BSA), 0,25 μM di substrato peptidico biotinilato (GGGGQDGKDYIVLPI) e da 1 a 30 μM di adenosina trifosfato (ATP) a seconda del Km per il rispettivo enzima. Le concentrazioni di ATP sono a o appena al di sotto del Km. Per le reazioni di c-KIT e FLT3 il pH viene aumentato a 7,5 con 0,2 a 8 μM di ATP in presenza di 0,25 a 1 μM di substrato peptidico biotinilato (GGLFDDPSYVNVQNL). Le reazioni vengono incubate a temperatura ambiente per 1-4 ore e il peptide fosforilato viene catturato su piastre a micropozze rivestite di streptavidina contenenti tampone di arresto della reazione (25 mM EDTA [acido etilendiamminotetraacetico], 50 mM HEPES, pH 7,5). Il peptide fosforilato viene misurato con il sistema DELFIA TRF utilizzando un anticorpo antifosfotirosina PT66 marcato con Europio. La concentrazione di Dovitinib per l'IC50 viene calcolata utilizzando la regressione non lineare con il software di analisi dei dati XL-Fit versione 4.1 (IDBS). L'inibizione dell'attività chinasica del recettore del fattore stimolante le colonie-1 (CSF-1R), PDGFRα, del recettore dell'insulina (InsR) e del recettore del fattore di crescita insulino-simile 1 (IGFR1) viene determinata a concentrazioni di ATP vicine al Km per ATP.
|
|
| In vivo |
Dovitinib induce risposte sia citostatiche che citotossiche in vivo, con conseguente regressione dei tumori che esprimono FGFR3. Dovitinib mostra un'inibizione dose- ed esposizione-dipendente dei recettori tirosina chinasi (RTK) target espressi negli xenotrapianti tumorali. Dovitinib inibisce potentemente la crescita tumorale di sei linee di HCC. L'inibizione dell'Angiogenesis è correlata all'inattivazione delle vie di segnalazione FGFR/PDGFRβ/VEGFR2. In un modello ortotopico, Dovitinib inibisce potentemente la crescita tumorale primaria e le metastasi polmonari e prolunga significativamente la sopravvivenza dei topi. La somministrazione di Dovitinib si traduce in una significativa inibizione della crescita tumorale e regressioni tumorali, inclusi tumori grandi e consolidati (500-1.000 mm3). |
Riferimenti |
|
Informazioni sullo studio clinico
(dati da https://clinicaltrials.gov, aggiornato il 2024-05-22)
| Numero NCT | Reclutamento | Condizioni | Sponsor/Collaboratori | Data di inizio | Fasi |
|---|---|---|---|---|---|
| NCT05571969 | Recruiting | Advanced Solid Tumors |
Allarity Therapeutics|Amarex Clinical Research |
February 20 2023 | Phase 1 |
| NCT02268435 | Withdrawn | Gastrointestinal Stromal Tumors |
Asan Medical Center |
March 2015 | Phase 1 |
| NCT01700270 | Completed | Advanced Solid Tumors Excluding Breast Cancer |
Novartis Pharmaceuticals|Novartis |
May 2013 | Phase 1 |
| NCT01680796 | Withdrawn | Multiple Myeloma |
University of Florida|Novartis Pharmaceuticals |
February 2013 | Phase 1 |
| NCT01266070 | Terminated | Von Hippel-Lindau Syndrome |
M.D. Anderson Cancer Center|Novartis |
November 2012 | Phase 2 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
