solo per uso di ricerca
Decitabine DNA Methyltransferase inibitore
N. Cat.S1200
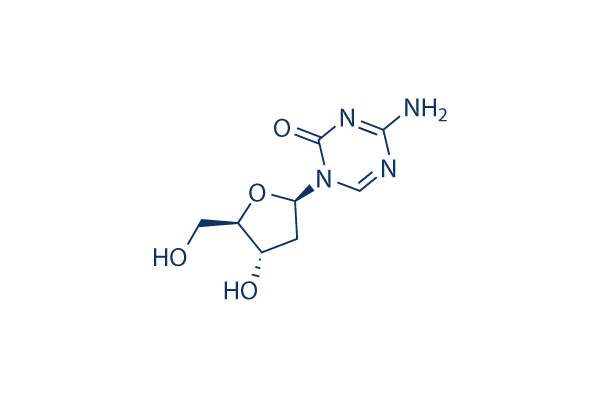
Struttura chimica
Peso molecolare: 228.21
Controllo Qualità
| Target correlati | HDAC JAK BET Histone Methyltransferase PKC PARP HIF PRMT EZH2 AMPK |
|---|---|
| Altro DNA Methyltransferase Inibitori | RG108 SGI-1027 Zebularine (NSC 309132) GSK3685032 Gamma-Oryzanol CM272 β-thujaplicin Bobcat339 DC-05 2'-Deoxy-5-Fluorocytidine |
Coltura cellulare, trattamento e concentrazione di lavoro
| Linee cellulari | Tipo di saggio | Concentrazione | Tempo di incubazione | Formulazione | Descrizione dellattività | PMID |
|---|---|---|---|---|---|---|
| Eca109 | Function Assay | 0.5 μM | 24 h | water | modulates the gene expression of MAGE-A members | 25123082 |
| Eca109 | Growth Inhibition Assay | 0.5/2.5/5 μM | 24/48/72 h | water | inhibits cell growth in both dose- and time- dependent manner | 25123082 |
| Eca109 | Function Assay | 0.5 μM | 6/12/24 h | water | inhibits cell migration | 25123082 |
| Eca109 | Function Assay | 0.5 μM | 24 h | water | inhibits cell invasion | 25123082 |
| Eca109 | Growth Inhibition Assay | 0.5 μM | 24 h | water | induces G2/M arrest in the cell cycle | 25123082 |
| Eca109 | Function Assay | 0.5/1 μM | 24 h | water | decreases expression of NF-κB2 and MMP2 | 25123082 |
| SW1116 | Growth Inhibition Assay | 0.5/1/2/5 μM | 48 h | DMSO | enhances the Gefitinib induced cell inhibition | 24874286 |
| LOVO | Growth Inhibition Assay | 0.5/1/2/5 μM | 48 h | DMSO | enhances the Gefitinib induced cell inhibition | 24874286 |
| SW1116 | Function Assay | 10 μM | 48 h | DMSO | increases the effective at inhibiting AKT and mTOR signaling pathways combined with gefitinib | 24874286 |
| LOVO | Function Assay | 10 μM | 48 h | DMSO | increases the effective at inhibiting AKT and mTOR signaling pathways combined with gefitinib | 24874286 |
| SW1116 | Apoptosis Assay | 10 μM | 48 h | DMSO | enhances Gefitinib-induced apoptosis | 24874286 |
| LOVO | Apoptosis Assay | 10 μM | 48 h | DMSO | enhances Gefitinib-induced apoptosis | 24874286 |
| RPMI-8226 | Apoptosis Assay | 1/2 μM | 48/72/96 h | DMSO | induces cell apoptosis | 24833108 |
| OPM-2 | Apoptosis Assay | 1/2 μM | 72/96/120 h | DMSO | induces cell apoptosis | 24833108 |
| JJN3 | Apoptosis Assay | 0.5/1 μM | 24/48 h | DMSO | induces cell apoptosis | 24833108 |
| NCI-H929 | Apoptosis Assay | 1/2 μM | 72/96/120 h | DMSO | induces cell apoptosis | 24833108 |
| RPMI-8226 | Growth Inhibition Assay | 1/2 μM | 24/48/72 h | DMSO | affects cell cycle progression negatively | 24833108 |
| OPM-2 | Growth Inhibition Assay | 1/2 μM | 24/48/72 h | DMSO | affects cell cycle progression negatively | 24833108 |
| JJN3 | Growth Inhibition Assay | 0.5/1 μM | 24/48/72 h | DMSO | affects cell cycle progression negatively | 24833108 |
| NCI-H929 | Growth Inhibition Assay | 1/2 μM | 24/48/72 h | DMSO | affects cell cycle progression negatively | 24833108 |
| HeLa | Kinase Assay | Ki=1000–5000 μM for hENT1 | 24780098 | |||
| HeLa | Kinase Assay | Ki=5.6 ± 0.5 μM for hENT2 | 24780098 | |||
| HeLa | Kinase Assay | Ki=21.6 ± 3.0 μM for hCNT1 | 24780098 | |||
| HeLa | Kinase Assay | Ki=14.4 ± 4.6 μM for hCNT3 | 24780098 | |||
| NB4 | Function Assay | 2.5/5/7.5/10 μM | 24 h | DMSO | increasea the expression of precursor miR-125a | 24484870 |
| CD4+ CD25− T | Function Assay | 1/5 μM | reduceS global DNA methylation | 24476360 | ||
| BV-173 | Apoptosis Assay | 0.25/0.5/0.75/1 μM | 48/72/96 h | PBS | induces cell apoptosis in both dose- and time- dependent manner | 24423613 |
| ML-1 | Apoptosis Assay | 0.25/0.5/0.75/1 μM | 48/72/96 h | PBS | induces cell apoptosis in both dose- and time- dependent manner | 24423613 |
| HL-60 | Apoptosis Assay | 0.25/0.5/0.75/1 μM | 48/72/96 h | PBS | induces cell apoptosis in both dose- and time- dependent manner | 24423613 |
| KG-1a | Apoptosis Assay | 0.25/0.5/0.75/1 μM | 48/72/96 h | PBS | induces cell apoptosis in both dose- and time- dependent manner | 24423613 |
| BV-173 | Function Assay | 250/500nM | 48 h | PBS | induces delayed and sustained ROS increase | 24423613 |
| CEM | Function Assay | 250/500nM | 48 h | PBS | induces delayed and sustained ROS increase | 24423613 |
| HL-60 | Function Assay | 250/500nM | 48 h | PBS | induces delayed and sustained ROS increase | 24423613 |
| ML-1 | Function Assay | 250/500nM | 48 h | PBS | induces delayed and sustained ROS increase | 24423613 |
| DLD-1 | Function Assay | 250/500nM | 48 h | PBS | do not induces delayed and sustained ROS increase | 24423613 |
| HCT-116 | Function Assay | 250/500nM | 48 h | PBS | do not induces delayed and sustained ROS increase | 24423613 |
| U937-A/E-9/14/18 | Apoptosis Assay | 0.01/0.1/1/10 μM | 48 h | induces cell apoptosis in a dose-dependent manner | 24300456 | |
| HT29 | Growth Inhibition Assay | 72 h | IC50=1400±179 μM | 24172061 | ||
| SW48 | Growth Inhibition Assay | 72 h | IC50=15.2±6.2 μM | 24172061 | ||
| HCT116 | Growth Inhibition Assay | 72 h | IC50=1.7±0.4 μM | 24172061 | ||
| HepG2 | Function Assay | 0.5/1 μM | 24 h | DMSO | up-regulated the relative OCTN2 mRNA and protein expression | 24146874 |
| LS174T | Function Assay | 0.5/1 μM | 24 h | DMSO | lead to an increase of OCTN2 levels | 24146874 |
| HepG2 | Apoptosis Assay | 1/10/100 μM | 7 d | DMSO | induces cell apoptosis in a dose-dependent manner | 24146874 |
| LS174T | Apoptosis Assay | 1/10/100 μM | 7 d | DMSO | induces cell apoptosis in a dose-dependent manner | 24146874 |
| QBC-939 | Apoptosis Assay | 1/10/100 μM | 7 d | DMSO | induces cell apoptosis in a dose-dependent manner | 24146874 |
| U251 | Apoptosis Assay | 1/10/100 μM | 7 d | DMSO | induces cell apoptosis in a dose-dependent manner | 24146874 |
| HL-60 | Growth Inhibition Assay | 1 μM | 48 h | increases G2-phase cell fraction | 24000324 | |
| MDA‑MB‑453 | Function Assay | 0.2/1 μM | 72 h | causes re-expression of claudin 1 | 23844228 | |
| HCC1569 | Function Assay | 0.2/1 μM | 72 h | causes re-expression of claudin 1 | 23844228 | |
| BT‑474 | Function Assay | 0.2/1 μM | 72 h | causes re-expression of claudin 1 | 23844228 | |
| AGS | Apoptosis Assay | 5/10/20/50 μM | 48 h | DMSO | inhibits the cell viability | 23582784 |
| A549 | Apoptosis Assay | 5/10/20/50 μM | 48 h | DMSO | inhibits the cell viability | 23582784 |
| AGS | Growth Inhibition Assay | 5/10/20/50 μM | 48 h | DMSO | induces G2/M phase arrest | 23582784 |
| Kasumi-1 | Apoptosis Assay | 0.5 μM | 48 h | decreases the cell viability co-treated with Tf-NP-sc | 23493348 | |
| OCI-AML3 | Apoptosis Assay | 2.5 μM | 48 h | decreases the cell viability co-treated with Tf-NP-sc | 23493348 | |
| MV4-11 | Apoptosis Assay | 2.5 μM | 48 h | decreases the cell viability co-treated with Tf-NP-sc | 23493348 | |
| NK | Cytotoxity Assay | 0.02-20 μM | 5 d | decreases the cytolytic activity of NK cells at intermediate concentrations resulting in a U-shaped dose–response curve | 23328088 | |
| NK | Apoptosis Assay | 0.02-20 μM | 5 d | decrease NK cell proliferation and viability as the concentration increased | 23328088 | |
| NK | Function Assay | 0.01-20 μM | 5 d | causes hypomethylation of NK cells in a dose–response | 23328088 | |
| MOLT4/DNR | Function Assay | 5 μM | 4 d | reduces ABCB1 mRNA expression | 23060570 | |
| Jurkat/DOX | Function Assay | 5 μM | 4 d | reduces ABCB1 mRNA expression | 23060570 | |
| MOLT4/DNR | Growth Inhibition Assay | 5 μM | 4 d | reduces the IC50 value for daunorubicin sensitivity | 23060570 | |
| Jurkat/DOX | Growth Inhibition Assay | 5 μM | 4 d | reduces the IC50 value for daunorubicin sensitivity | 23060570 | |
| ccRCC | Apoptosis Assay | 0.01-10μM | 72 h | DMSO | has minimal effect on cell proliferation | 22826467 |
| TNBC | Apoptosis Assay | 0.01-10μM | 72 h | DMSO | has minimal effect on cell proliferation | 22826467 |
| A498 | Apoptosis Assay | 0.01-10μM | 72 h | DMSO | induces synergistic responses with romidepsin | 22826467 |
| KIJ265T | Apoptosis Assay | 0.01-10μM | 72 h | DMSO | induces synergistic responses with romidepsin | 22826467 |
| MDA-231 | Apoptosis Assay | 0.01-10μM | 72 h | DMSO | induces synergistic responses with romidepsin | 22826467 |
| BT-20 | Apoptosis Assay | 0.01-10μM | 72 h | DMSO | induces synergistic responses with romidepsin | 22826467 |
| U937 | Growth Inhibition Assay | 5-20 μM | 24/48/72 h | induces a decrease in cell viability in a concentration- and time-dependent manner | 22767021 | |
| HL60 | Growth Inhibition Assay | 5-20 μM | 24/48/72 h | induces a decrease in cell viability in a concentration- and time-dependent manner | 22767021 | |
| U937 | Apoptosis Assay | 15 μM | 24/48/72 h | induces cell apoptosis | 22767021 | |
| HL60 | Apoptosis Assay | 15 μM | 24/48/72 h | induces cell apoptosis | 22767021 | |
| LS411N | Apoptosis Assay | 0.5 μM | 72 h | increases Fas mRNA level | 22461695 | |
| MDA-MB-231 | Apoptosis Assay | 10 μM | 48 h | reduces cell viability in a dose-dependent manner | 21887697 | |
| MCF-7 | Apoptosis Assay | 10 μM | 48 h | reduces cell viability in a dose-dependent manner | 21887697 | |
| A375 | Growth Inhibition Assay | 0.5 μM | 1/5/8 d | inhibits proliferation and induces differentiation of melanoma cells | 21796622 | |
| SKMEL1 | Growth Inhibition Assay | 0.5 μM | 1/5/8 d | inhibits proliferation and induces differentiation of melanoma cells | 21796622 | |
| SKMEL3 | Growth Inhibition Assay | 0.5 μM | 1/5/8 d | inhibits proliferation and induces differentiation of melanoma cells | 21796622 | |
| SKMEL28 | Growth Inhibition Assay | 0.5 μM | 1/5/8 d | inhibits proliferation and induces differentiation of melanoma cells | 21796622 | |
| MeWo | Growth Inhibition Assay | 0.5 μM | 1/5/8 d | inhibits proliferation and induces differentiation of melanoma cells | 21796622 | |
| B16 | Growth Inhibition Assay | 0.5 μM | 1/5/8 d | inhibits proliferation and induces differentiation of melanoma cells | 21796622 | |
| Ly 1 | Growth Inhibition Assay | 24 h | IC50=7.3 μM | 21772049 | ||
| Ly 7 | Growth Inhibition Assay | 24 h | IC50=10.7 μM | 21772049 | ||
| Su-DHL6 | Growth Inhibition Assay | 24 h | IC50>20 μM | 21772049 | ||
| Ly 10 | Growth Inhibition Assay | 24 h | IC50>20 μM | 21772049 | ||
| RIVA | Growth Inhibition Assay | 24 h | IC50>20 μM | 21772049 | ||
| Su-DHL2 | Growth Inhibition Assay | 24 h | IC50>20 μM | 21772049 | ||
| Ly 1 | Growth Inhibition Assay | 48 h | IC50=0.34 μM | 21772049 | ||
| Ly 7 | Growth Inhibition Assay | 48 h | IC50=0.025 μM | 21772049 | ||
| Su-DHL6 | Growth Inhibition Assay | 48 h | IC50>20 μM | 21772049 | ||
| Ly 10 | Growth Inhibition Assay | 48 h | IC50=1.8 μM | 21772049 | ||
| RIVA | Growth Inhibition Assay | 48 h | IC50>20 μM | 21772049 | ||
| Su-DHL2 | Growth Inhibition Assay | 48 h | IC50=17.4 μM | 21772049 | ||
| Ly 1 | Growth Inhibition Assay | 72 h | IC50=0.01 μM | 21772049 | ||
| Ly 7 | Growth Inhibition Assay | 72 h | IC50=0.018 μM | 21772049 | ||
| Su-DHL6 | Growth Inhibition Assay | 72 h | IC50=1.6 μM | 21772049 | ||
| Ly 10 | Growth Inhibition Assay | 72 h | IC50=1.2 μM | 21772049 | ||
| RIVA | Growth Inhibition Assay | 72 h | IC50>20 μM | 21772049 | ||
| Su-DHL2 | Growth Inhibition Assay | 72 h | IC50=11.2 μM | 21772049 | ||
| U373-MAGI | Antiviral assay | 0.25 to 8 uM | 2 to 72 hrs | Antiviral activity against VSV-G pseudotyped HIV-1 NL4-3 infected in human U373-MAGI cells assessed as reduction in U5-gag level at 0.25 to 8 uM after 2 to 72 hrs by qPCR method | 27117260 | |
| U373-MAGI | Antiviral assay | 0.25 to 8 uM | 2 to 72 hrs | Antiviral activity against VSV-G pseudotyped HIV-1 NL4-3 infected in human U373-MAGI cells assessed as reduction in gag level at 0.25 to 8 uM after 2 to 72 hrs by qPCR method | 27117260 | |
| Clicca per visualizzare più dati sperimentali sulle linee cellulari | ||||||
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 228.21 | Formula | C8H12N4O4 |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 2353-33-5 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
| Sinonimi | Deoxycytidine, 5-aza-2'-deoxycytidine, 5-AZA-dC, 5-aza-CdR,NSC 127716 | Smiles | C1C(C(OC1N2C=NC(=NC2=O)N)CO)O | ||
Solubilità
|
In vitro |
DMSO
: 45 mg/mL
(197.18 mM)
Water : 22.5 mg/mL Ethanol : Insoluble |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Targets/IC50/Ki |
DNA methylation
(HL-60, KG1a cells) |
|---|---|
| In vitro |
Decitabine inibisce la crescita cellulare in modo dose- e tempo-dipendente con IC50 di circa 438 nM e 43,8 nM per esposizioni di 72 ore e 96 ore nelle cellule leucemiche HL-60 e KG1a, rispettivamente. Uno studio recente mostra che questo composto esibisce un'elevata attività antiproliferativa e pro-apoptotica contro il linfoma anaplastico a grandi cellule (ALCL), e inibisce l'assorbimento di [3H]–timidina nelle cellule KARPAS-299 con una EC50 di 0,49 μM. |
| Saggio chinasico |
saggio di sintesi del DNA
|
|
Il tasso di sintesi del DNA è misurato dall'incorporazione di timidina radioattiva nel DNA. Le cellule HL-60 e KG1a vengono sospese in 2 mL di terreno RPMI contenente il 10% di siero fetale in piastre a 6 pozzetti (35 mm di diametro) e incubate con diverse concentrazioni dei farmaci corrispondenti per 48 ore (i farmaci vengono aggiunti contemporaneamente). A 48 ore, 0,5 μCi di [3H] timidina (6,7 Ci/mmol) viene aggiunta a ciascun pozzetto e incubata per ulteriori 24 ore. Le cellule vengono poste su filtri in fibra di vetro GF/C (2,4 cm di diametro), lavate con NaCl freddo 0,9%, acido tricloroacetico freddo 5% ed etanolo. I filtri contenenti il DNA vengono quindi essiccati, posti in liquido di scintillazione EcoLite (ICN) e la radioattività misurata utilizzando un contatore a scintillazione Beckman LS 6000IC. L'IC50 è definita come la concentrazione del farmaco che inibisce il 50% della sintesi del DNA delle linee cellulari leucemiche dalla curva dose-risposta.
|
|
| In vivo |
In un modello di xenotrapianto murino ALK+ KARPAS-299, Decitabine a una dose di 2,5 mg/kg provoca un aumento dell'apoptosi e una riduzione della proliferazione delle cellule tumorali, e comporta anche la demetilazione del soppressore tumorale p16INK4A. |
Riferimenti |
|
Applicazioni
| Metodi | Biomarcatori | Immagini | PMID |
|---|---|---|---|
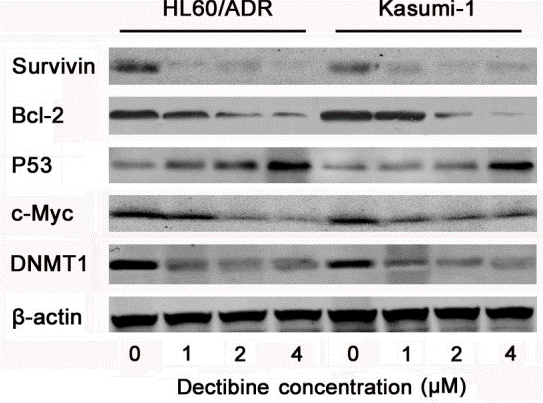
| Western blot | Survivin / Bcl-2 / p53 / c-Myc / DNMT1 p-AKT / AKT / p-GSK3β / GSK3β / p-Myc / Myc / p-P70 / P70 / p-4EBP-1 / 4EBP-1 / PTEN phospho-p38 / p38 / phospho-NFκB / NFκB p-JAK1 / JAK1 / p-JAK2 / JAK2 / p-STAT3 / STAT3 E-cadherin / N-cadherin / Snail / MMP-2 / MMP-9 / Bcl-2 / Bax |
|
26384351 |
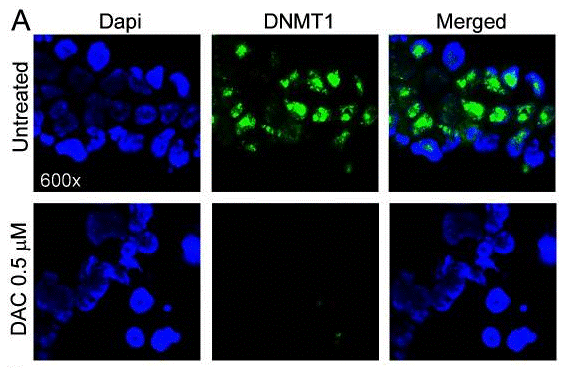
| Immunofluorescence | DNMT1 E-cadherin / MMP-9 |
|
21303982 |
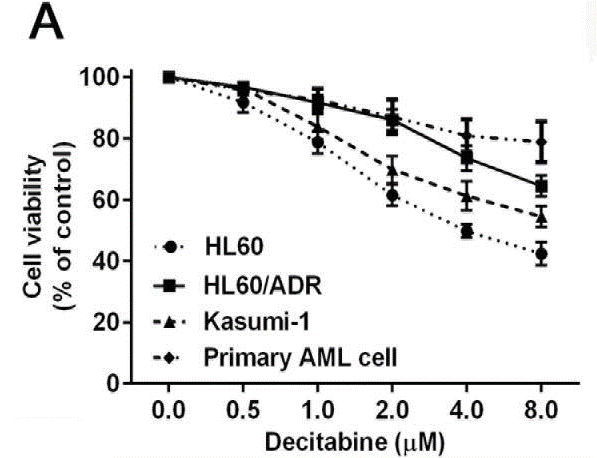
| Growth inhibition assay | Cell viability |
|
26384351 |
Informazioni sullo studio clinico
(dati da https://clinicaltrials.gov, aggiornato il 2024-05-22)
| Numero NCT | Reclutamento | Condizioni | Sponsor/Collaboratori | Data di inizio | Fasi |
|---|---|---|---|---|---|
| NCT06291285 | Not yet recruiting | Healthy Volunteers |
Novo Nordisk A/S |
February 27 2024 | Phase 1 |
| NCT05960773 | Recruiting | Mesothelioma|Malignant Mesothelioma (MM)|Early-stage Mesothelioma|Subclinical Mesothelioma|BRCA1-Associated Protein-1 (BAP1) Mutations|Early-stage BAP1-associated Malignancies |
National Cancer Institute (NCI)|National Institutes of Health Clinical Center (CC) |
January 31 2024 | Phase 2 |
| NCT05835011 | Terminated | Myelodysplastic Syndromes |
Astex Pharmaceuticals Inc. |
July 14 2023 | Phase 2 |
| NCT05816356 | Recruiting | Healthy |
EpiDestiny Inc.|Worldwide Clinical Trials |
March 24 2023 | Phase 1 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
Domande Frequenti
Domanda 1:
Is it a racemic mixture or a monomer?
Risposta:
Its S1200 is R form.
