solo per uso di ricerca
UNC1999 Histone Methyltransferase inibitore
N. Cat.S7165
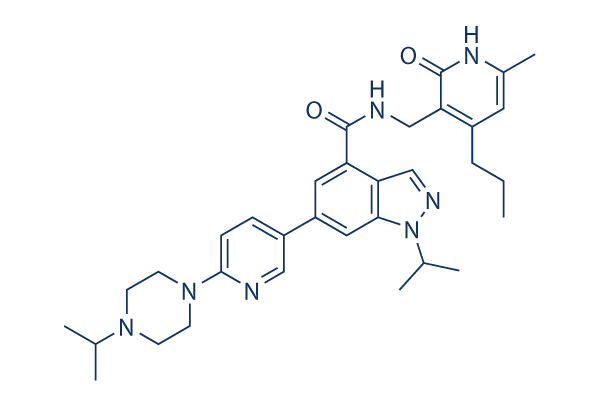
Struttura chimica
Peso molecolare: 569.74
Controllo Qualità
| Target correlati | HDAC JAK BET PKC PARP HIF PRMT EZH2 AMPK Histone Acetyltransferase |
|---|---|
| Altro Histone Methyltransferase Inibitori | Pinometostat (EPZ5676) 3-Deazaneplanocin A (DZNep) Hydrochloride BIX-01294 trihydrochloride EPZ015666 (GSK3235025) EPZ004777 MM-102 (HMTase Inhibitor IX) Chaetocin SGC 0946 EPZ005687 UNC0638 |
Coltura cellulare, trattamento e concentrazione di lavoro
| Linee cellulari | Tipo di saggio | Concentrazione | Tempo di incubazione | Formulazione | Descrizione dellattività | PMID |
|---|---|---|---|---|---|---|
| human MCF10A cells | Function assay | 72 h | Inhibition of EZH2 in human MCF10A cells assessed as reduction of H3K27me3 level after 72 hrs by Western blot analysis, IC50=0.124 μM | 25406853 | ||
| human MCF10A cells | Cytotoxic assay | Cytotoxicity against human MCF10A cells assessed as cell viability by Alamar Blue assay, EC50=19.2 μM | 25406853 | |||
| Clicca per visualizzare più dati sperimentali sulle linee cellulari | ||||||
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 569.74 | Formula | C33H43N7O2 |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 1431612-23-5 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
| Sinonimi | N/A | Smiles | CCCC1=C(C(=O)NC(=C1)C)CNC(=O)C2=C3C=NN(C3=CC(=C2)C4=CN=C(C=C4)N5CCN(CC5)C(C)C)C(C)C | ||
Solubilità
|
In vitro |
DMSO
: 100 mg/mL
(175.51 mM)
Ethanol : 100 mg/mL Water : Insoluble |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Caratteristiche |
The first orally bioavailable inhibitor against wild-type and mutant EZH2 as well as EZH1.
|
|---|---|
| Targets/IC50/Ki |
EZH2
(Cell-free assay) 2 nM
EZH1
(Cell-free assay) 45 nM
|
| In vitro |
UNC1999 è altamente potente per i mutanti EZH2 Y641N e EZH2 Y641F in vitro. Questo composto provoca riduzioni dose-dipendenti di H3K27me3 nelle cellule MCF10A con IC50 di 124 nM, pur mostrando bassa tossicità cellulare. Mostra una potente inibizione dose-dipendente della proliferazione cellulare con EC50 di 633 nM in una linea cellulare di DLBCL che ospita il mutante EZH2Y641N. Inoltre, UNC1999 biotinilato arricchisce EZH2 dai lisati cellulari di HEK293T, e quindi può essere utilizzato in studi di chemioproteomica.
|
| Saggio chinasico |
Saggio di prossimità a scintillazione
|
|
I saggi di attività della metiltransferasi vengono eseguiti monitorando l'incorporazione del gruppo metilico marcato con trizio da S-adenosilmetionina (3H-SAM) a substrati peptidici biotinilati utilizzando il Saggio di Prossimità a Scintillazione (SPA) per il complesso trimerico PRC2-EZH2 (EZH2:EED:SUZ12), il complesso pentamerico PRC2-EZH1 (EZH1:EED:SUZ12:RBBP4:AEBP2), SETD7, G9a, GLP, SETDB1, SETD8, SUV420H1, SUV420H2, SUV39H2, il complesso tetramerico MLL1 (MLL:WDR5:RbBP5:ASH2L), PRMT1, PRMT3, il complesso PRMT5-MEP50 e SMYD2. Il tampone di reazione per SMYD2 e SMYD3 è 50 mM Tris pH 9.0, 5 mM DTT, 0.01% TritonX-100; per G9a, GLP e SUV39H2 è 25 mM fosfato di potassio pH 8.0, 1 mM EDTA, 2 mM MgCl2 e 0.01% Triton X-100; e per altre HMT 20 mM Tris pH 8.0, 5 mM DTT, 0.01% TritonX-100. Per arrestare le reazioni enzimatiche, vengono aggiunti 10 μL di guanidina cloridrato 7.5 M, seguiti da 180 μL di tampone, miscelati e trasferiti in una FlashPlate a 384 pozzetti. Dopo la miscelazione, le miscele di reazione vengono incubate e i conteggi CPM vengono misurati utilizzando un lettore di piastre Topcount. I conteggi CPM in assenza di questo composto per ogni set di dati sono definiti come attività al 100%. In assenza dell'enzima, i conteggi CPM in ogni set di dati sono definiti come sfondo (0%). I valori di IC50 vengono determinati utilizzando concentrazioni di composto che vanno da 100 nM a 100 μM. I valori di IC50 vengono determinati utilizzando il software SigmaPlot. I saggi EZH2-Y641F vengono eseguiti utilizzando 30 nM di enzima in 20 mM Tris pH 8, 5 mM DTT, 0.01% Triton X-100, 5 μM SAM e 1 μM di peptide H3 (1-24) (lo stesso che per il complesso PRC2-EZH2 di tipo selvatico). Per DNMT1, il saggio viene eseguito utilizzando dsDNA emimetilato come substrato. Il substrato di dsDNA viene preparato mediante annealing di due filamenti complementari (filamento avanti biotinilato: BGAGCCCGTAAGCCCGTTCAGGTCG e filamento inverso: CGACCTGAACGGGCTTACGGGCTC), sintetizzati da Eurofins MWG Operon. Il tampone di reazione è 20 mM Tris-HCl, pH 8.0, 5mM DTT, 0.01% Triton X-100. I saggi di attività della metiltransferasi per DOT1L vengono eseguiti utilizzando piastre filtranti. Le miscele di reazione in 20 mM Tris-HCl, pH 8.0, 5 mM DTT, 2 mM MgCl2 e 0.01% Triton X-100 vengono incubate a temperatura ambiente per 1h, vengono aggiunti 100 μL di TCA al 10%, miscelati e trasferiti in una piastra filtrante. Le piastre vengono centrifugate a 2000 rpm per 2 min seguite da 2 ulteriori lavaggi con TCA al 10% e un lavaggio con etanolo (180 μL) seguito da centrifugazione. Le piastre vengono essiccate e vengono aggiunti 100 μL di MicroO e centrifugate. Vengono aggiunti 70 μL di MicroO e i CPM vengono misurati utilizzando un lettore di piastre Topcount.
|
|
| In vivo |
Il trattamento con UNC1999 (150 e 50 mg/kg, i.p.) si traduce in concentrazioni plasmatiche di questo composto superiori alla sua IC50 cellulare per oltre 24 ore in vivo. Inoltre, è anche biodisponibile per via orale nei topi, il che rende gli studi sugli animali cronici più pratici e convenienti.
|
Riferimenti |
|
Applicazioni
| Metodi | Biomarcatori | Immagini | PMID |
|---|---|---|---|
| Western blot | H3K27Me3 / Cleaved PARP / LC3B H3K27me2 / H3K27me1 / H3K27ac / H3K4me3 / H3K9me2 / H3K36me2 |
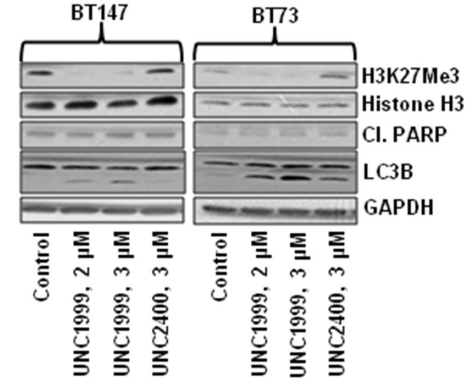
|
27449082 |
| Immunofluorescence | EZH2 / H3K27me3 NF-κB |
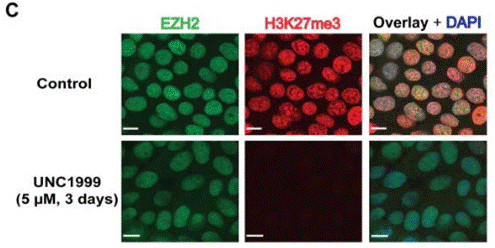
|
23614352 |
| Growth inhibition assay | Cell viability |
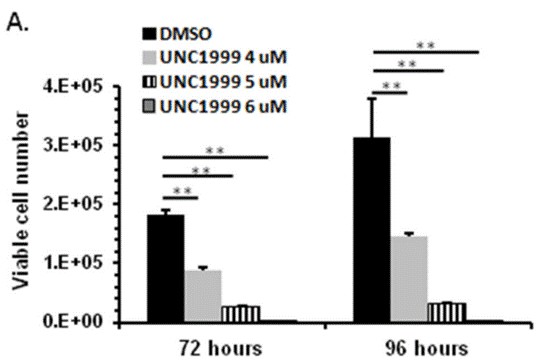
|
27449082 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
