solo per uso di ricerca
AEE788 (NVP-AEE788) EGFR inibitore
N. Cat.S1486
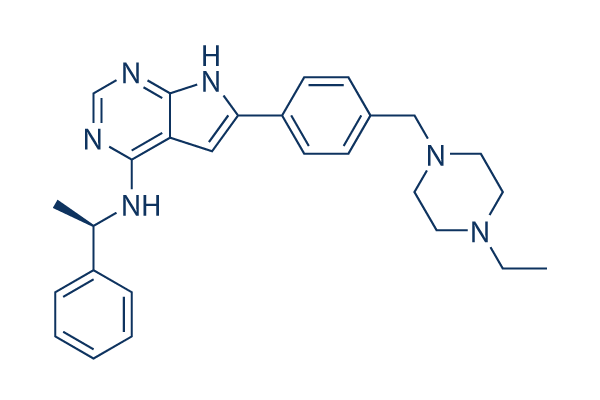
Struttura chimica
Peso molecolare: 440.58
Controllo Qualità
| Target correlati | VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Altro EGFR Inibitori | Lazertinib (YH25448) Icotinib Hydrochloride Sunvozertinib AG-490 AG-1478 Canertinib (CI-1033) WZ4002 Rociletinib (CO-1686) Poziotinib (NOV120101, HM781-36B) Genistein |
Coltura cellulare, trattamento e concentrazione di lavoro
| Linee cellulari | Tipo di saggio | Concentrazione | Tempo di incubazione | Formulazione | Descrizione dellattività | PMID |
|---|---|---|---|---|---|---|
| Huh7 | Cytotoxicity assay | Cytotoxicity against human hepatocellular carcinoma cell line (Huh7), CC50=27.83 Μm | ||||
| Jeko B cells | Function assay | 2 h | Inhibition of PI3Kdelta in human Jeko B cells assessed as inhibition of Akt phosphorylation after 2 hrs, IC50=0.017 μM | |||
| Clicca per visualizzare più dati sperimentali sulle linee cellulari | ||||||
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 440.58 | Formula | C27H32N6 |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 497839-62-0 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
| Sinonimi | N/A | Smiles | CCN1CCN(CC1)CC2=CC=C(C=C2)C3=CC4=C(N3)N=CN=C4NC(C)C5=CC=CC=C5 | ||
Solubilità
|
In vitro |
DMSO
: 88 mg/mL
(199.73 mM)
Water : Insoluble Ethanol : Insoluble |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Targets/IC50/Ki |
EGFR
(Cell-free assay) 2 nM
HER2/ErbB2
(Cell-free assay) 6 nM
c-Abl
(Cell-free assay) 52 nM
FLT1
(Cell-free assay) 59 nM
c-Fms
(Cell-free assay) 60 nM
c-Src
(Cell-free assay) 61 nM
KDR
(Cell-free assay) 77 nM
HER4/ErbB4
(Cell-free assay) 160 nM
|
|---|---|
| In vitro |
AEE788 (NVP-AEE788) inibisce anche KDR, c-abl, c-Src e Flt-1 con IC50 di 50-80 nM. Non è sensibile a ErbB-4, PDGFR-β, Flt-3, Flt-4, RET e c-Kit e non ha azione inibitoria su Ins-R, IGF-1R, PKC-α e PKA. Questo composto inibisce potentemente la fosforilazione di EGFR nelle cellule A431 con IC50 di 11 nM. Inibisce anche la fosforilazione di KDR nelle cellule CHO e di erbB2 nelle cellule BT-474, senza alcun effetto sulla fosforilazione indotta da PDGF nelle cellule A31. Inibisce la proliferazione delle cellule NCI-H596, MK, BT-474 e SK-BR-3 con IC50 di 78, 56, 49 e 381 nM, rispettivamente. Inoltre, ha la proprietà aggiuntiva di inibire la proliferazione cellulare guidata dal mutante EGFR, inclusi 32D/EGFR e 32D/EGFRvIII. Inoltre, inibisce la proliferazione delle HUVEC sia indotta da EGF che da VEGF con IC50 di 43 e 155 nM, rispettivamente. Inibisce la fosforilazione di EGFR, VEGFR2, Akt e MAPK nelle linee cellulari di SCC cutaneo umano (cellule Colo16, HaCaT, SRB1 e SRB12), il che porta all'inibizione della crescita e all'induzione dell'apoptosi. Inibisce la fosforilazione di EGFR e Akt nelle cellule HT29 a 0,2-1,0 μM. Inibisce la proliferazione cellulare e previene l'attivazione di HER1, HER2 e HER3 indotta da EGF e neuregulina nelle linee cellulari di medulloblastoma. Mostra attività soppressive della crescita nelle cellule di medulloblastoma chemio-sensibili e chemio-resistenti.
|
| Saggio chinasico |
Saggi di Protein Kinase
|
|
I saggi in vitro di Protein Tyrosine Kinase per AEE788 (NVP-AEE788) vengono eseguiti in piastre a 96 pozzetti (30 μL) a temperatura ambiente per 15–45 min utilizzando i domini chinasi ricombinanti fusi alla glutatione S-transferasi (4-100 ng, a seconda dell'attività specifica). Il [γ33P]ATP è utilizzato come donatore di fosfato e il peptide poliGluTyr-(4:1) come accettore. Con l'eccezione della Protein Kinase C-α, la chinasi ciclina-dipendente 1/cycB e la Protein Kinase A sono rispettivamente solfato di protamina (200 μg/mL), istone H1 (100 μg/mL) e l'eptapeptide Leu-Arg-Arg-Ala-Ser-Leu-Gly (noto come Kemptide Bachem) e sono utilizzati come substrati peptidici. I saggi sono ottimizzati per ogni chinasi utilizzando le seguenti concentrazioni di ATP: 1,0 μM (c-Kit, c-Met, c-Fms, c-Raf-1 e RET), 2,0 μM (EGFR, erbB2, ErbB3 ed ErbB4), 5,0 μM (c-abl), 8,0 μM (Flt-1, Flt-3, Flt-4, Flk, KDR, FGFR-1 e Tek), 10,0 μM (PDGFR-β, Protein Kinase C-α e chinasi ciclina-dipendente 1) e 20,0 μM (c-Src e Protein Kinase A). La reazione viene terminata con l'aggiunta di 20 μL di EDTA 125 mM. Trenta μL (c-abl, c-Src, recettore del fattore di crescita 1 insulino-simile, RET-Men2A e RET-Men2B) o 40 μL (tutte le altre chinasi) della miscela di reazione vengono trasferiti su una membrana di Immobilon-polivinilidene difluoruro, pre-immersa in H3PO4 allo 0,5% e montata su un collettore a vuoto. Viene quindi applicato il vuoto e ogni pozzetto viene risciacquato con 200 μL di H3PO4 allo 0,5%. Le membrane vengono rimosse e lavate quattro volte con H3PO4 all'1,0% e una volta con etanolo. Le membrane essiccate vengono contate dopo essere state montate in un telaio Packard TopCount a 96 pozzetti e con l'aggiunta di 10 μL/pozzetto di Microscint. I valori di IC50 (±SE) sono calcolati mediante analisi di regressione lineare della percentuale di inibizione e sono medie di almeno tre determinazioni.
|
|
| In vivo |
AEE788 (NVP-AEE788) produce un'inibizione dose-dipendente della crescita tumorale in modelli di xenotrapianto NCI-H596 o DU145, con solo lievi modifiche del peso corporeo. Induce la regressione tumorale del 57% a 50 mg/kg nel modello NeuT/erbB2 GeMag e inibisce potentemente la fosforilazione di EGFR indotta da EGF nei tumori A431 e la fosforilazione di erbB2 nei tumori GeMag. Questo composto ha inibito in modo dose-dipendente l'angiogenesi indotta da VEGF e non inibisce l'angiogenesi indotta da bFGF. Sopprime la crescita del volume tumorale del 54% negli xenotrapianti Colo16 a 50 mg/kg, il che è dovuto all'inibizione della fosforilazione di EGFR, VEGFR, Akt e MAPK. A 50 mg/kg, inibisce anche la crescita dei tumori nel cieco e nel peritoneo (>50%) e riduce l'incidenza delle metastasi linfonodali al 70% nelle cellule HT29 impiantate nel cieco di topi nudi, senza perdita di peso corporeo e prove macroscopiche di neovascolarizzazione. Abbassa significativamente i livelli di espressione di pEGFR e pVEGFR nei tumori cecali HT29 e non altera quelli di EGF, VEGF, EGFR o VEGFR. Combinato con CPT-11, si traduce in tumori significativamente più piccoli e inibizione completa delle metastasi linfonodali. Questo composto inibisce la crescita degli xenotrapianti Daoy, DaoyPt e DaoyHER2 rispettivamente del 51%, 45% e 72%. Potrebbe promuovere la generazione di specie reattive dell'ossigeno mediate da LBH589 nelle cellule tumorali K562, che a sua volta aumenta l'apoptosi.
|
Riferimenti |
|
Informazioni sullo studio clinico
(dati da https://clinicaltrials.gov, aggiornato il 2024-05-22)
| Numero NCT | Reclutamento | Condizioni | Sponsor/Collaboratori | Data di inizio | Fasi |
|---|---|---|---|---|---|
| NCT00107237 | Completed | Brain and Central Nervous System Tumors |
Novartis Pharmaceuticals|Novartis |
October 2003 | Phase 1|Phase 2 |
| NCT00118456 | Completed | Cancer |
Novartis Pharmaceuticals|Novartis |
July 2003 | Phase 1 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
