solo per uso di ricerca
AG-490 EGFR inibitore
N. Cat.S1143
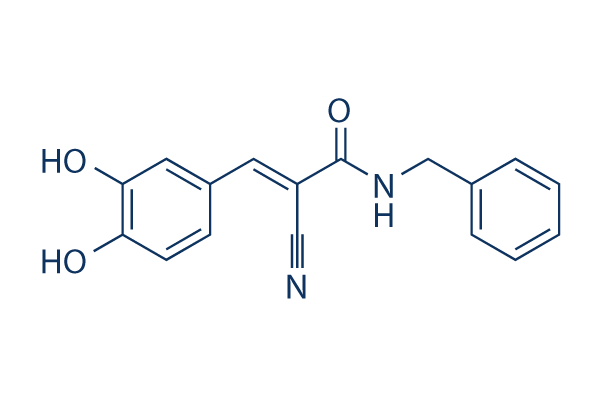
Struttura chimica
Peso molecolare: 294.30
Controllo Qualità
| Target correlati | VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Altro EGFR Inibitori | Lazertinib (YH25448) Icotinib Hydrochloride Sunvozertinib AG-1478 Canertinib (CI-1033) WZ4002 Rociletinib (CO-1686) Poziotinib (NOV120101, HM781-36B) Genistein Allitinib tosylate |
Coltura cellulare, trattamento e concentrazione di lavoro
| Linee cellulari | Tipo di saggio | Concentrazione | Tempo di incubazione | Formulazione | Descrizione dellattività | PMID |
|---|---|---|---|---|---|---|
| BC3 | Function Assay | 100 µM | 24 h | mediates PEL cell apoptosis | ||
| BCBL1 | Function Assay | 100 µM | 24 h | mediates PEL cell apoptosis | ||
| BC3 | Function Assay | 100 µM | 24 h | mediates de-phosphorylation of STAT3 correlated with HSP70 and HSF1 reduction | ||
| BCBL1 | Function Assay | 100 µM | 24 h | mediates de-phosphorylation of STAT3 correlated with HSP70 and HSF2 reduction | ||
| BC3 | Function Assay | 100 µM | 24 h | induces a complete autophagic flux | ||
| BCBL1 | Function Assay | 100 µM | 24 h | induces a complete autophagic flux | ||
| SK-MEL-28 | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| MeWo | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| SK-MEL-5 | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| SK-MEL-2 | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| B16-F0 | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| TRPM2/HEK | Function Assay | 0.1–25 µM | 15 min | DMSO | reduces H2O2-induced Ca2+increase in a concentration-dependent manner, and the IC50 value was 1.7 µM | |
| U937 | Function Assay | 0.1–25 µM | 15 min | DMSO | reduces H2O2-induced Ca2+increase in a concentration-dependent manner, and the IC50 value was 0.4 µM | |
| TRPM2/HEK | Function Assay | 10 µM | 40 min | DMSO | reduces TRPM2 activation even at high concentrations of H2O2 | |
| GL37 | Cell Viability Assay | 0-10 µM | 48 h | suppresses La expression | ||
| NRK-52E | Function Assay | 1 µM | 10 min | blocks the stimulatory effect of Ang II on Pax-2 expression | ||
| NRK-52E | Function Assay | 1 µM | 10 min | blocks Ang II induced CD24 expression | ||
| HSC | Function Assay | 20 μM | 1 h | abrogates the differential effects of leptin or AGEs | ||
| EJ | Growth Inhibition Assay | 50/80 μM | 24/48/72 h | inhibits cell growth in both time and dose dependent manner | ||
| EJ | Growth Inhibition Assay | 50/80 μM | 48 h | causes S-phase arrest | ||
| EJ | Function Assay | 50/80 μM | 48 h | downregulates c-Myc, cyclinD1, survivin and VEGF expressions | ||
| HepG2 | Function Assay | 50-500 μM | 60 min | inhibits the IL-6-induced phosphorylation of STAT1 (Tyr705) and STAT3 (Tyr705) in a dose-dependent manner | ||
| SGC7901 | Cell Viability Assay | 0-100 μM | 24/48/72 h | causes a significant reduction in cell viability dose-dependently but not time-dependently | ||
| AGS | Cell Viability Assay | 0-100 μM | 24/48/72 h | causes a significant reduction in cell viability dose-dependently but not time-dependently | ||
| SGC7901 | Function Assay | 50 μM | 24/48/72 h | the levels of pJAK2 began to decline at 24 hr, and rebounded at 72 hr | ||
| AGS | Function Assay | 50 μM | 24/48/72 h | the levels of pJAK2 began to decline at 24 hr, and rebounded at 72 hr | ||
| SGC7901 | Function Assay | 50 μM | 24/48/72 h | the cytoplasmic localization of pJAK2 (JAK2 phosphorylated at residues Tyr1007 and Tyr1008) decreased after AG490 treatment for 24 and 48 hr, but started to rebound at 72 hr | ||
| AGS | Function Assay | 50 μM | 24/48/72 h | the cytoplasmic localization of pJAK2 (JAK2 phosphorylated at residues Tyr1007 and Tyr1008) decreased after AG490 treatment for 24 and 48 hr, but started to rebound at 72 hr | ||
| MC3T3-E1 | Function Assay | 50 μM | 4 h | inhibits HSE-induced BMP7 and GHR protein expression | ||
| 7TD1-DXM | Growth Inhibition Assay | 10 μM | 72 h | DMSO | inhibits cell growth | |
| 7TD1-WD-90 | Growth Inhibition Assay | 10 μM | 72 h | DMSO | inhibits cell growth | |
| 7TD1-DXM | Apoptosis Assay | 50 μM | 48 h | DMSO | induces apoptosis | |
| 7TD1-WD-90 | Apoptosis Assay | 50 μM | 48 h | DMSO | induces apoptosis | |
| 7TD1-WD-90 | Function Assay | 50 μM | 6 h | DMSO | significantly inhibits the phosphorylation of JAK2 and phosphorylation of STAT3 | |
| HepG2 | Function Assay | 100 μM | 12/24 h | inhibits STAT3 tyrosine phosphorylation | ||
| RAW264.7 | Function Assay | 50 μM | 24/48 h | suppresses RANKL-induced osteoclastogenesis | ||
| RAW264.7 | Growth Inhibition Assay | 0-50 μM | 48 h | inhibits cell growth dose-dependently | ||
| RAW264.7 | Growth Inhibition Assay | 0-50 μM | 48 h | causes an arrest of RAW264.7 cells at the G0/G1 phase of the cell cycle | ||
| RAW264.7 | Function Assay | 50 μM | 24/48 h | inhibits RANKL-induced NFATc1 expression and phosphorylation of Ser727STAT3 | ||
| A549 | Function Assay | 20/40 μM | 20 h | 20 μM AG490 suppresses the radiation-induced invasion of A549 cells | ||
| A549 | Function Assay | 10/20/40 μM | 24 h | suppresses the radiation-induced elevation of VEGF | ||
| HUVECs | Cell Viability Assay | 20 µM | 4 h | attenuates H2O2-induced cell shrinkage and improved the attachment rate of the cells | ||
| HUVECs | Apoptosis Assay | 20 µM | 4 h | significantly decreases the cell apoptotic index | ||
| BV-2 | Function Assay | 20 µM | 16 h | inhibits LPS-induced STAT1 phosphorylation with almost completely diminished iNOS expression | ||
| NRK-52E | Function Assay | 5 μM | 30 min | attenuates Ang-(1–7)-inhibited TGF-β1 mRNA at 16 h | ||
| SW620 | Function Assay | 20 µM | 1/6 h | inhibits p-STAT3 activation | ||
| RPE | Function Assay | 30 µM | 3 h | inhibits the induction of p-STAT3 expression | ||
| SW1116 | Function Assay | 100 µM | 24/48/72 h | decreases the expression of JAK2 and pJAK2 time-dependently | ||
| HT29 | Function Assay | 100 µM | 24/48/72 h | decreases the expression of JAK2 and pJAK2 time-dependently | ||
| SW1116 | Function Assay | 100 µM | 24/48/72 h | decreases the pSTAT3 levels in a time-dependent manner | ||
| HT29 | Function Assay | 100 µM | 24/48/72 h | decreases the pSTAT3 levels in a time-dependent manner | ||
| ARPE-19 | Function Assay | 5 μM | 30 min | inhibits JAK2 phosphorilation | ||
| HSC-T6 | Apoptosis Assay | 10 μM | 2 h | inhibits the apoptosis of HSC-T6 cells induced by CDE | ||
| HSC-T6 | Function Assay | 10 μM | 2 h | inhibits the expressions of pY-STAT1 and Bad induced by CDE | ||
| Hep-2 | Growth Inhibition Assay | 25-100 μM | 24/48/72 h | inhibits cell growth in both time and dose dependent manner | ||
| Hep-2 | Apoptosis Assay | 50 μM | 24/48/72 h | induces cell apoptosis time dependently | ||
| Hep-2 | Function Assay | 50 μM | 24/48/72 h | inhibits G1 to S cell cycle transition and induces G1 cell cycle arrest | ||
| Hep-2 | Function Assay | 50 μM | 24/48/72 h | downregulates the STAT3, p-STAT3 and survivin protein levels | ||
| KF8 | Function Assay | 10 μM | 1 h | DMSO | inhibits IL-33-induced NF-κB activation | |
| KF8 | Function Assay | 10 μM | 1 h | DMSO | inhibits IL-33-induced IκBα degradation and NF-κB activation | |
| HEL | Function Assay | 100 μM | 12-72 h | inhibits the level of p-JAK2, JAK2 | ||
| HEL | Growth Inhibition Assay | 100 μM | 0-5 d | reduces growth of JAK2V617F-expressing HEL cells | ||
| A-172 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| MZ-18 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| MZ-54 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| MZ-256 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| MZ-304 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| A-172 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| MZ-18 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| MZ-54 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| MZ-256 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| MZ-304 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| A-172 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| MZ-18 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| MZ-54 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| MZ-256 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| MZ-304 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| A-172 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| MZ-18 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| MZ-54 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| MZ-256 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| MZ-304 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| A-172 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| MZ-18 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| MZ-54 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| MZ-256 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| MZ-304 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| SW1990 | Growth Inhibition Assay | 20 μM | 24/48/72 h | inhibits cell growth time dependently | ||
| SW1990 | Function Assay | 20 μM | 24 h | decreases the expression of MMP-2 and VEGF mRNAs | ||
| SW1990 | Function Assay | 20 μM | 24 h | decreases the intensity of p-Stat3 expression | ||
| SW1990 | Invasion Assay | 20 μM | 24 h | reduces invasion of SW1990 cells | ||
| THP1 | Function Assay | 10 uM | 30 min | inhibits STAT3 tyrosine phosphorylation by over 60% | ||
| BMMC | Function Assay | 0-10 μM | 15 min | inhibits LTC4 release in a dose-dependent fashion with near complete inhibition at concentrations ⩾10 μM | ||
| A549 | Function Assay | 15 μm | 1 h | inhibits the phosphorylation of STAT1 on tyrosine 701 was detected 15 min after SPE B treatment | ||
| OVCAR-3 | Function Assay | 10 uM | 1 h | inhibits LPA-induced STAT3 phosphorylation | ||
| PA-1 | Function Assay | 10 uM | 1 h | inhibits LPA-induced STAT3 phosphorylation | ||
| OVCAR-3 | Function Assay | 10 uM | 1 h | inhibits LPA-induced ovarian cancer cell motility | ||
| PA-1 | Function Assay | 10 uM | 1 h | inhibits LPA-induced ovarian cancer cell motility | ||
| Jurkat | Growth Inhibition Assay | 50 μM | 24/48/72 h | enhances TRAIL-induces cell growth inhibition | ||
| SUPT1 | Growth Inhibition Assay | 50 μM | 24/48/72 h | enhances TRAIL-induces cell growth inhibition | ||
| Jurkat | Apoptosis Assay | 50 μM | 24/48 h | enhances TRAIL-induces cell apoptosis | ||
| SUPT1 | Apoptosis Assay | 50 μM | 24/48 h | enhances TRAIL-induces cell apoptosis | ||
| Clicca per visualizzare più dati sperimentali sulle linee cellulari | ||||||
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 294.30 | Formula | C17H14N2O3 |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 133550-30-8 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
| Sinonimi | Tyrphostin B42, Zinc02557947 | Smiles | C1=CC=C(C=C1)CNC(=O)C(=CC2=CC(=C(C=C2)O)O)C#N | ||
Solubilità
|
In vitro |
DMSO
: 58 mg/mL
(197.07 mM)
Ethanol : 9 mg/mL Water : Insoluble |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Targets/IC50/Ki |
JAK2 (V617F)
EGFR
(Cell-free assay) 0.1 μM
|
|---|---|
| In vitro |
AG-490 inibisce la proliferazione cellulare indotta da HER-2 con IC50 di 3,5 μM. Corrispondente alla specifica inibizione dose-dipendente di JAK2 costitutivamente attivato nelle cellule di leucemia acuta pre-B (ALL), questo composto (5 μM) blocca quasi completamente la crescita di tutte le cellule ALL inducendo la morte cellulare programmata, senza effetti deleteri sull'ematopoiesi normale. Questa sostanza chimica non inibisce le attività di Lck, Lyn, Btk, Syk e Src. Esso (60-100 μM) blocca l'attivazione costitutiva di Stat3sm e inibisce la crescita spontanea e quella indotta dall'interleuchina 2 delle cellule tumorali di micosi fungoide (MF) con valori di IC50 rispettivamente di 75 μM e 20 μM. Questo composto inibisce potentemente la crescita delle cellule T umane mediata da IL-2 con un IC50 di 25 μM bloccando le attività di JAK3 e STAT5a/b. Inibisce significativamente l'attivazione costitutiva di Stat3 nelle cellule MOPC, MPC11 e S194, portando a una drammatica apoptosi dose-dipendente. Questa sostanza chimica (100 μM) inibisce la fosforilazione di Akt, inibisce l'attivazione del fattore nucleare-κB e causa l'attivazione di GSK-3β, portando alla riduzione di c-Myc. Essa (50 μM) può indurre l'apoptosi delle cellule BaF3 che esprimono i mutanti T315I ed E255K di Bcr-Abl. Questo composto a 30 μM inibisce non solo la fosforilazione di JAK2 wild-type indotta da Epo, ma anche la fosforilazione costitutiva del mutante JAK2 V617F. Inibisce anche potentemente la crescita cellulare indipendente dalle citochine indotta dal mutante JAK2 V617F nelle cellule BaF3. |
| Saggio chinasico |
Autofosforilazione chinasica in vitro
|
|
AG-490 viene disciolto in DMSO 10%-H2O-etanolo 45%. Estratti di membrana grezzi (0,125 μg/mL) vengono preattivati con EGF (20 nM) in tampone HEPES 50 mM, pH 7,6, e NaCl 125 mM, per 15 minuti a 4 °C. L'attività di autofosforilazione della chinasi EGFR o ErbB2 viene saggiata a 4 °C per 30 secondi in piastre a 96 pozzetti a forma di V. Estratti di membrana (8 μL) vengono aggiunti a ciascun pozzetto contenente la miscela di reazione (12 μL, HEPES 50 mM, pH 7,4, NaCl 125 mM, M8Ac2 12 mM, MnCl2 2 mM, NaVO3 1 mM, ATP 1 μM e 1 μCi [γ-32P]ATP, concentrazioni finali) e concentrazioni crescenti di questo composto (4 μL). Dopo la terminazione mediante aggiunta di tampone campione caldo, i campioni vengono eseguiti su un minigel di elettroforesi su gel di poliacrilammide SDS al 6%, i gel vengono essiccati e viene eseguita l'autoradiografia durante il periodo di tempo di esposizione lineare. Le bande del recettore vengono scansionate densitrometricamente e i risultati analizzati dal programma Ez-Fit. Per l'analisi dell'autofosforilazione di JAK2, JAK2 viene immunoprecipitata utilizzando un anticorpo anti-JAK2 da lisati di cellule G2 pretrattate per 16 ore con concentrazioni crescenti di questa sostanza chimica (0-50 μM). I complessi immuni vengono quindi immunoblottati con un anticorpo anti-fosfotirosina. Un'inibizione dose-dipendente dell'attività chinasica in vitro è dimostrata valutando l'autofosforilazione di JAK2.
|
|
| In vivo |
L'amministrazione di AG-490 riduce drasticamente il numero di cellule CD45+ e HLA-DR+ dal 48 % e 46 % nel midollo osseo di topi non trattati, così come dal 38 % e 22 % nella milza di topi non trattati, a livelli non rilevabili. L'amministrazione in vivo di questo composto causa l'apoptosi delle cellule tumorali di mieloma murino ma non inibisce l'attivazione dei macrofagi mediata da IL-12 e la produzione di IFN-γ da parte dei linfociti. Coerentemente con il blocco in vitro dell'attività del mutante JAK2 V617F, il trattamento con questa sostanza chimica a 0,5 mg/giorno per 10 giorni inibisce efficacemente la tumorigenesi e l'invasione delle cellule tumorali indotte dal mutante JAK2 V617F nei topi nudi. La terapia combinata con questo agente e IL-12 induce effetti antitumorali maggiori rispetto a ciascun agente da solo in un modello murino di tumore di mieloma. |
Riferimenti |
|
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
Domande Frequenti
Domanda 1:
I would like to know whether it (S1143) goes to CNS through BBB, or not?
Risposta:
It can go through the BBB, as shown in this reference: http://bloodjournal.hematologylibrary.org/content/111/4/2062.full.html.
