Dati tecnici
| Formula | C27H32N6 |
||||||||||
| Peso molecolare | 440.58 | Numero CAS | 497839-62-0 | ||||||||
| Solubilità (25°C)* | In vitro | DMSO | 88 mg/mL (199.73 mM) | ||||||||
| Ethanol | 6 mg/mL (13.61 mM) | ||||||||||
| Water | Insoluble | ||||||||||
| In vivo (Aggiungere i solventi al prodotto singolarmente e in ordine.) |
|
||||||||||
|
* <1 mg/ml significa leggermente solubile o insolubile. * Si prega di notare che Selleck testa la solubilità di tutti i composti internamente e la solubilità effettiva può differire leggermente dai valori pubblicati. Ciò è normale ed è dovuto a leggere variazioni da lotto a lotto. * Spedizione a temperatura ambiente (I test di stabilità mostrano che questo prodotto può essere spedito senza alcuna misura di raffreddamento.) |
|||||||||||
Preparazione delle soluzioni stock
Attività biologica
| Descrizione | AEE788 (NVP-AEE788) è un potente inibitore di EGFR e HER2/ErbB2 con IC50 di 2 nM e 6 nM, rispettivamente. È meno potente contro VEGFR2/KDR, c-Abl, c-Src e Flt-1 e non inibisce Ins-R, IGF-1R, PKCα o CDK1. Questo composto ha raggiunto gli studi clinici di Fase 1/2. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Target |
|
|||||||||||
| In vitro | AEE788 (NVP-AEE788) inibisce anche KDR, c-abl, c-Src e Flt-1 con IC50 di 50-80 nM. Non è sensibile a ErbB-4, PDGFR-β, Flt-3, Flt-4, RET e c-Kit e non ha azione inibitoria su Ins-R, IGF-1R, PKC-α e PKA. Questo composto inibisce potentemente la fosforilazione di EGFR nelle cellule A431 con IC50 di 11 nM. Inibisce anche la fosforilazione di KDR nelle cellule CHO e di erbB2 nelle cellule BT-474, senza alcun effetto sulla fosforilazione indotta da PDGF nelle cellule A31. Inibisce la proliferazione delle cellule NCI-H596, MK, BT-474 e SK-BR-3 con IC50 di 78, 56, 49 e 381 nM, rispettivamente. Inoltre, ha la proprietà aggiuntiva di inibire la proliferazione cellulare guidata dal mutante EGFR, inclusi 32D/EGFR e 32D/EGFRvIII. Inoltre, inibisce la proliferazione delle HUVEC sia indotta da EGF che da VEGF con IC50 di 43 e 155 nM, rispettivamente. Inibisce la fosforilazione di EGFR, VEGFR2, Akt e MAPK nelle linee cellulari di SCC cutaneo umano (cellule Colo16, HaCaT, SRB1 e SRB12), il che porta all'inibizione della crescita e all'induzione dell'apoptosi. Inibisce la fosforilazione di EGFR e Akt nelle cellule HT29 a 0,2-1,0 μM. Inibisce la proliferazione cellulare e previene l'attivazione di HER1, HER2 e HER3 indotta da EGF e neuregulina nelle linee cellulari di medulloblastoma. Mostra attività soppressive della crescita nelle cellule di medulloblastoma chemio-sensibili e chemio-resistenti. | |||||||||||
| In vivo | AEE788 (NVP-AEE788) produce un'inibizione dose-dipendente della crescita tumorale in modelli di xenotrapianto NCI-H596 o DU145, con solo lievi modifiche del peso corporeo. Induce la regressione tumorale del 57% a 50 mg/kg nel modello NeuT/erbB2 GeMag e inibisce potentemente la fosforilazione di EGFR indotta da EGF nei tumori A431 e la fosforilazione di erbB2 nei tumori GeMag. Questo composto ha inibito in modo dose-dipendente l'angiogenesi indotta da VEGF e non inibisce l'angiogenesi indotta da bFGF. Sopprime la crescita del volume tumorale del 54% negli xenotrapianti Colo16 a 50 mg/kg, il che è dovuto all'inibizione della fosforilazione di EGFR, VEGFR, Akt e MAPK. A 50 mg/kg, inibisce anche la crescita dei tumori nel cieco e nel peritoneo (>50%) e riduce l'incidenza delle metastasi linfonodali al 70% nelle cellule HT29 impiantate nel cieco di topi nudi, senza perdita di peso corporeo e prove macroscopiche di neovascolarizzazione. Abbassa significativamente i livelli di espressione di pEGFR e pVEGFR nei tumori cecali HT29 e non altera quelli di EGF, VEGF, EGFR o VEGFR. Combinato con CPT-11, si traduce in tumori significativamente più piccoli e inibizione completa delle metastasi linfonodali. Questo composto inibisce la crescita degli xenotrapianti Daoy, DaoyPt e DaoyHER2 rispettivamente del 51%, 45% e 72%. Potrebbe promuovere la generazione di specie reattive dell'ossigeno mediate da LBH589 nelle cellule tumorali K562, che a sua volta aumenta l'apoptosi. |
Protocollo (da riferimento)
| Saggio della chinasi:[1] |
|
|---|---|
| Saggio cellulare:[1] |
|
| Studio sugli animali:[1] |
|
Riferimenti
|
Convalida del prodotto da parte del cliente
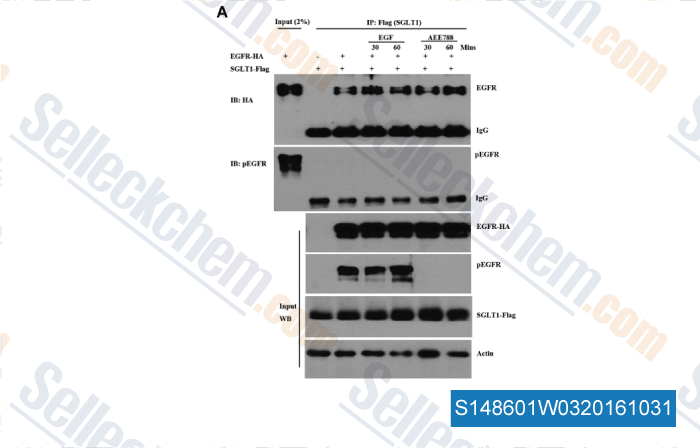
-
, , The Prostate, 2013, 73:1453-1461.
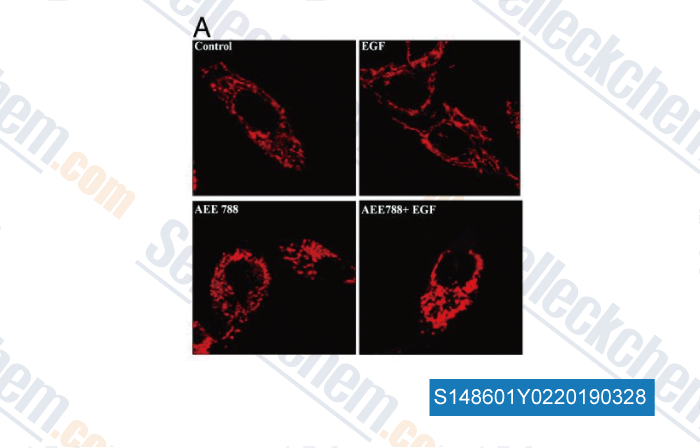
-
Dati da [ , , Cell Cycle, 2014, 13(15):2415-30 ]
Sellecks AEE788 (NVP-AEE788) È stato citato da 13 Pubblicazioni
| A community challenge for a pancancer drug mechanism of action inference from perturbational profile data [ Cell Rep Med, 2022, 3(1):100492] | PubMed: 35106508 |
| Comprehensive pharmacogenomic characterization of gastric cancer. [ Genome Med, 2020, 18;12(1):17] | PubMed: 32070411 |
| Targeting the non-canonical roles of PCNA modifies and increases the response to targeted anti-cancer therapy [ Oncotarget, 2019, 10(68):7185-7197] | PubMed: 31921382 |
| Rationale for Using Irreversible Epidermal Growth Factor Receptor Inhibitors in Combination with Phosphatidylinositol 3-Kinase Inhibitors for Advanced Head and Neck Squamous Cell Carcinoma. [ Mol Pharmacol, 2019, 95(5):528-536] | PubMed: 30858165 |
| Targeted reduction of the EGFR protein, but not inhibition of its kinase activity, induces mitophagy and death of cancer cells through activation of mTORC2 and Akt. [ Oncogenesis, 2018, 7(1):5] | PubMed: 29358623 |
| Synergistic induction of apoptosis by salinomycin and gefitinib through lysosomal and mitochondrial dependent pathway overcomes gefitinib resistance in colorectal cancer. [ Oncotarget, 2017, 8(14):22414-22432] | PubMed: 26461472 |
| A high-content EMT screen identifies multiple receptor tyrosine kinase inhibitors with activity on TGFβ receptor [ Oncotarget, 2016, 7(18-:25983-6002] | PubMed: 27036020 |
| [ Oncotarget, 2015, ] | PubMed: 25965827 |
| [ Oncotarget, 2015, ] | PubMed: 26378037 |
| Phosphorylation of Mutationally Introduced Tyrosine in the Activation Loop of HER3 Confers Gain-of-Function Activity [Hu Z, et al. PLoS One, 2015, 10(4):e0123623] | PubMed: 25853726 |
POLITICA DI RESO
La politica di reso incondizionato di Selleck Chemical garantisce ai nostri clienti unesperienza di acquisto online senza problemi. Se non sei in alcun modo soddisfatto del tuo acquisto, puoi restituire qualsiasi articolo entro 7 giorni dalla ricezione. In caso di problemi di qualità del prodotto, sia relativi al protocollo che al prodotto, puoi restituire qualsiasi articolo entro 365 giorni dalla data di acquisto originale. Si prega di seguire le istruzioni seguenti per la restituzione dei prodotti.
SPEDIZIONE E CONSERVAZIONE
I prodotti Selleck vengono trasportati a temperatura ambiente. Se ricevi il prodotto a temperatura ambiente, ti assicuriamo che il Dipartimento di Ispezione Qualità di Selleck ha condotto esperimenti per verificare che la conservazione a temperatura normale per un mese non influirà sullattività biologica dei prodotti in polvere. Dopo la raccolta, conservare il prodotto secondo le indicazioni descritte nella scheda tecnica. La maggior parte dei prodotti Selleck è stabile nelle condizioni raccomandate.
NON PER USO UMANO, DIAGNOSTICO VETERINARIO O TERAPEUTICO.
