solo per uso di ricerca
Ruxotemitide (LTX 315) Bcl-2 modulatore
N. Cat.S8199
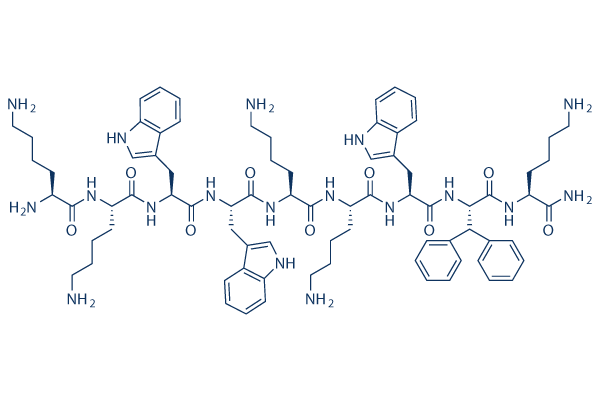
Struttura chimica
Peso molecolare: 1439.79
Controllo Qualità
| Target correlati | Caspase PD-1/PD-L1 Ferroptosis p53 Apoptosis related Synthetic Lethality STAT TNF-alpha Ras KRas |
|---|---|
| Altro Bcl-2 Inibitori | Navitoclax (ABT-263) S63845 ABT-737 Obatoclax Mesylate (GX15-070) A-1331852 A-1210477 TW-37 A-1155463 Dihydrochloride AZD5991 UMI-77 |
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 1439.79 | Formula | C78H106N18O9 |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 1345407-05-7 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
Solubilità
|
In vitro |
Water : 100 mg/mL |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| In vitro |
LTX-315 è altamente attivo contro le linee cellulari di melanoma murino e umano in vitro, pur mostrando una bassa attività citotossica EC50 contro i globuli rossi umani. È stato dimostrato che LTX-315 induce il rilascio di ATP e HMGB1 in vitro, entrambi DAMP coinvolti nell'ICD.
|
|---|---|
| In vivo |
Quando i melanomi B16 singenici vengono trattati per via intralesionale, la maggior parte degli animali (~80%) trattati con LTX-315 sperimenta una regressione tumorale completa e duratura. L'iniezione di LTX-315 induce un'estesa necrosi emorragica del parenchima tumorale e una massiccia infiltrazione di cellule T CD3+, indicando che il peptide induce un tipo di morte cellulare che porta a un aumento del numero di linfociti infiltranti il tumore (TIL). Il trattamento di un singolo tumore con LTX-315 genera una risposta immunitaria antitumorale sistemica che ha eradicato le lesioni distanti e prevenuto la ricomparsa dopo una nuova sfida tumorale.
|
Riferimenti |
|
Applicazioni
| Metodi | Biomarcatori | Immagini | PMID |
|---|---|---|---|
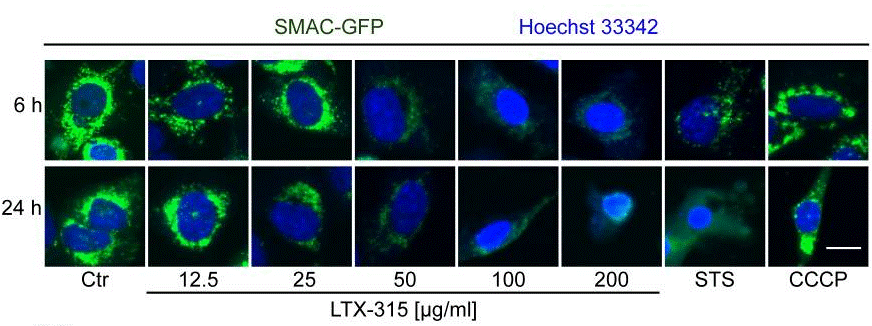
| Immunofluorescence | SMAC BAX |
|
26378049 |
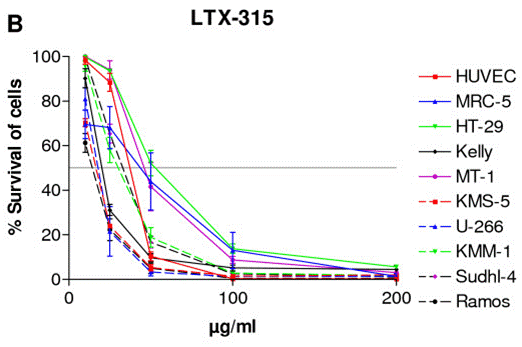
| Growth inhibition assay | Cell viability |
|
21453492 |
Informazioni sullo studio clinico
(dati da https://clinicaltrials.gov, aggiornato il 2024-05-22)
| Numero NCT | Reclutamento | Condizioni | Sponsor/Collaboratori | Data di inizio | Fasi |
|---|---|---|---|---|---|
| NCT03725605 | Completed | Soft Tissue Sarcoma |
Lytix Biopharma AS|Herlev Hospital |
December 28 2018 | Phase 2 |
| NCT01223209 | Completed | Carcinoma |
Lytix Biopharma AS|Kael-GemVax Co. Ltd. |
August 2010 | Phase 1 |
| NCT01058616 | Completed | Cancer With Transdermal Accessible Tumour |
Lytix Biopharma AS|Oslo University Hospital|Karolinska University Hospital |
January 2010 | Phase 1 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
