solo per uso di ricerca
Apigenin P450 (e.g. CYP17) inibitore
N. Cat.S2262
Struttura chimica
Peso molecolare: 270.24
Controllo Qualità
| Target correlati | Dehydrogenase HSP Transferase PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism Drug Metabolite |
|---|---|
| Altro P450 (e.g. CYP17) Inibitori | Baicalein Avasimibe Naringenin Diosmetin Alizarin Orteronel Benzbromarone Sodium Danshensu Naringin Piperine |
Coltura cellulare, trattamento e concentrazione di lavoro
| Linee cellulari | Tipo di saggio | Concentrazione | Tempo di incubazione | Formulazione | Descrizione dellattività | PMID |
|---|---|---|---|---|---|---|
| mouse RAW264.7 cells | Function assay | Inhibition of COX2 protein expression in mouse RAW264.7 cells, IC50=0.5 μM | ||||
| human H295R cells | Function assay | Inhibition of aromatase expressed in human H295R cells, IC50=1 μM | ||||
| HEK293 FS cells | Function assay | Inhibition of NOX4 expressed in HEK293 FS cells assessed as H2O2 production by H2O2/Tyr/LPO assay, IC50=1.13 μM | ||||
| human HeLa cells | Function assay | Inhibition of MRP1 transfected in human HeLa cells assessed as inhibition of [3H]LTC4 transport by rapid filtration assay, Ki=2.4 μM | ||||
| human MV4-11 cells | Cytotoxicity assay | 72 h | Cytotoxicity against human MV4-11 cells harboring FLT3 mutation after 72 hrs by tetrazolium based Ez CyTox cell viability assay, GI50=2.81 μM | |||
| human mast cells | Function assay | Inhibition of SYK in human mast cells assessed as reduction in mast cell degranulation, EC50=3 μM | ||||
| MDCK cells | Function assay | Inhibition of BCRP expressed in MDCK cells using Hoechst 33342 staining, IC50=3.1 μM | ||||
| human MDA-kb2 cells | Function assay | Antagonist activity at androgen receptor in human MDA-kb2 cells assessed as inhibition of DHT-induced luciferase activity by luciferase reporter gene assay, IC50=5.2 μM | ||||
| MCF-7 MX cells | Function assay | Inhibition of BCRP expressed in MCF-7 MX cells using Hoechst 33342 staining, IC50=5.9 μM | ||||
| mouse RAW264.7 cells | Function assay | 24 h | Antiinflammatory activity against mouse RAW264.7 cells assessed as inhibition of LPS-induced nitrite accumulation after 24 hrs by Griess reagent method, IC50=6.7 μM | |||
| human H9 cells | Function assay | 3 days | Antiviral activity against HIV1 3B infected in human H9 cells assessed as inhibition of viral replication after 3 days by p24 antigen capture assay, EC50=9 μM | |||
| HEK293 cells | Function assay | 24 h | Agonist activity at mouse PPARgamma expressed in HEK293 cells co-expressing with Gal4 reporter vector after 24 hrs by dual-luciferase reporter assay, EC50=24.9 μM | |||
| mouse 26-L5 cells | Proliferation assay | 72 h | Antiproliferative activity against mouse 26-L5 cells after 72 hrs by MTT assay, EC50=25 μM | |||
| human RS4:11 cells | Cytotoxicity assay | 72 h | Cytotoxicity against human RS4:11 cells harboring wild type FLT3 after 72 hrs by tetrazolium based Ez CyTox cell viability assay, GI50=27.9 μM | |||
| mouse B16-BL6 cells | Proliferation assay | 72 h | Antiproliferative activity against mouse B16-BL6 cells after 72 hrs by MTT assay, EC50=31.6 μM | |||
| human H9 cells | Cytotoxicity assay | 3 days | Cytotoxicity against human H9 cells after 3 days, IC50=35 μM | |||
| human HT1080 cells | Proliferation assay | 72 h | Antiproliferative activity against human HT1080 cells after 72 hrs by MTT assay, IC | |||
| MDCK cells | Cytotoxicity assay | Cytotoxicity against MDCK cells by MTT assay, CC50=39.59 μM | ||||
| mouse L929 cells | Function assay | 15 mins | Potentiation of recombinant human TNF-alpha-induced cytotoxicity of mouse L929 cells assessed as survivality preincubated for 15 mins before TNFalpha addition measured after 24 hrs by crystal violet staining | |||
| human THP1 cells | Function assay | 20 uM | 1 h | Inhibition of NOX2 in human THP1 cells assessed as downregulation of TPA-induced CD36 mRNA expression at 20 uM incubated for 1 hr prior to TPA challenge measured after 24 hrs by RT-PCR analysis | ||
| MDA-MB-231 cells | Function assay | 5 uM | Inhibition of PMA-stimulated NF-kappaB signaling (unknown origin) expressed in MDA-MB-231 cells at 5 uM incubated for 16 hrs by luciferase reporter gene assay | |||
| Clicca per visualizzare più dati sperimentali sulle linee cellulari | ||||||
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 270.24 | Formula | C15H10O5 |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 520-36-5 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
Solubilità
|
In vitro |
DMSO
: 54 mg/mL
(199.82 mM)
Water : Insoluble Ethanol : Insoluble |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Caratteristiche |
Much more potent than kaempferol and myricetin in CT-L inhibition.
|
|---|---|
| Targets/IC50/Ki |
CYP2C9
2 μM(Ki)
|
| In vitro |
Apigenin inibisce la PKC competendo con l'adenosina trifosfato (ATP). Questo composto riduce anche il livello di fosforilazione delle proteine cellulari stimolata dal TPA e inibisce l'espressione di c-jun e c-fos indotta dal TPA. Esibisce l'effetto di inversione sulla morfologia trasformata delle cellule NIH3T3 trasformate da v-H-ras. È stato dimostrato che possiede proprietà antimutagene in un contesto di genotossicità indotta da nitropirene in cellule ovariche di criceto cinese. Questa sostanza chimica sopprime l'attività e l'espressione della cicloossigenasi-2 e della nitrossido sintasi-2 indotte da LPS nei macrofagi murini. È stato riportato che inibisce l'attività della proteina chinasi C, la chinasi proteica attivata dai mitogeni (MAPK), la trasformazione dei fibroblasti embrionali di topo C3HI e gli oncogeni a valle nelle cellule NIH3T3 trasformate da v-Ha-ras. Questo composto blocca la chinasi regolata dalla proliferazione dei perossisomi (ERK), una MAPK negli epatociti isolati. È stato inoltre dimostrato che regola negativamente l'espressione dell'antiportatore Na+/Ca2+, una proteina importante per l'estrusione del calcio nei miociti cardiaci di ratto neonatale. Induce un arresto reversibile in G2/M e G0/G1 inibendo l'attività della chinasi p34 (cdc2), accompagnato da una maggiore stabilità della proteina p53 nelle cellule epidermiche e nei fibroblasti. È anche efficace nell'inibire la sovraregolazione della molecola di adesione intracellulare-1 indotta da TNFα nelle cellule endoteliali umane coltivate. Inibisce l'espressione di HIF-1α e VEGF tramite le vie PI3K/Akt/p70S6K1 e HDM2/p53 nelle cellule di cancro ovarico umano. Inibisce la differenziazione sopprimendo la trasduzione del segnale MAPK e riducendo il livello del fattore di trascrizione API nei cheratinociti umani. Questo composto inibisce anche la proliferazione dei cheratinociti umani.
|
| In vivo |
Apigenin regola negativamente la produzione di IL-4 in topi BALB/C immunizzati con ovoalbumina. Questo composto inibisce le metastasi polmonari del melanoma alterando l'interazione delle cellule tumorali con l'endotelio. È stato dimostrato che causa un aumento significativo del peso uterino e della concentrazione uterina complessiva del recettore degli estrogeni (ER)-α in topi femmine (64) e sopprime anche la crescita delle cellule tumorali della prostata e del seno tramite il recettore degli estrogeni β1. Questa sostanza chimica sopprime i livelli di IGF-I negli xenotrapianti di tumore alla prostata e aumenta i livelli di IGFBP-3, una proteina legante che sequestra l'IGF-I nella circolazione vascolare. Questo composto (12,5 mg/kg) aumenta la proliferazione cellulare nel giro dentato dell'ippocampo di topi adulti.
|
Riferimenti |
|
Applicazioni
| Metodi | Biomarcatori | Immagini | PMID |
|---|---|---|---|
| Western blot | MHC / MHC2A / MHC2B / MyoD CXCR4 CDK1 / Cyclin B1 / p21 |

|
29108230 |
| Immunofluorescence | E-caherin / Vimentin Snail |
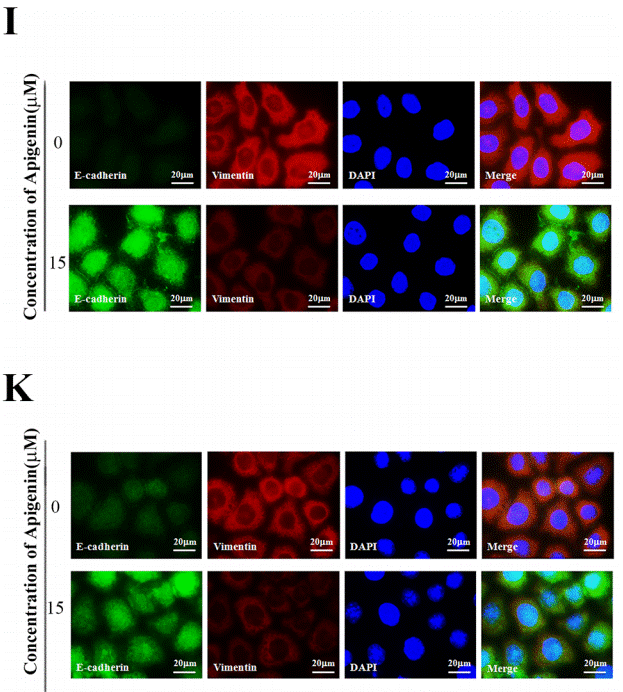
|
27203387 |
| Growth inhibition assay | Cell viability |
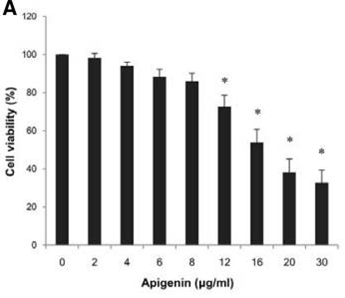
|
23224239 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
