solo per uso di ricerca
NSC 23766 Trihydrochloride Inibitore di Rac GTPase
N. Cat.S8031
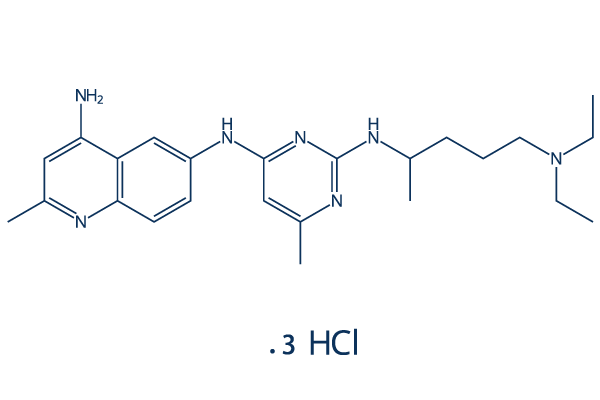
Struttura chimica
Peso molecolare: 530.97
Controllo Qualità
| Target correlati | CDK HSP PD-1/PD-L1 ROCK Wee1 DNA/RNA Synthesis Microtubule Associated Ras KRas Aurora Kinase |
|---|---|
| Altro Rho Inibitori | EHop-016 CCG-1423 ML141 (CID-2950007) EHT 1864 2HCl ZCL278 MBQ-167 CCG-203971 Rhosin hydrochloride CID44216842 1A-116 |
Coltura cellulare, trattamento e concentrazione di lavoro
| Linee cellulari | Tipo di saggio | Concentrazione | Tempo di incubazione | Formulazione | Descrizione dellattività | PMID |
|---|---|---|---|---|---|---|
| RA4 | Function Assay | 50 μM | 24 h | inhibits Matrigel invasion | 17622308 | |
| RA3 | Function Assay | 50 μM | 24 h | inhibits Matrigel invasion | 17622308 | |
| RA2 | Function Assay | 50 μM | 24 h | inhibits Matrigel invasion | 17622308 | |
| RA1 | Function Assay | 50 μM | 24 h | inhibits Matrigel invasion | 17622308 | |
| RA-FLS (RA2) | Growth Inhibition Assay | 25/50 μM | 1-9 d | inhibits cell growth in both dose and time dependent manner | 17622308 | |
| IEC-6 | Function Assay | 120 µM | 4/6/8 h | prevents the increased activation of FAK at 6 and 8 h | 20448461 | |
| MDA-MB-231 | Function Assay | 50/100 μM | 48 h | induces a dose-dependent decrease in phosphorylation of p65 subunit | 20515940 | |
| MDA-MB-468 | Function Assay | 50/100 μM | 48 h | induces a dose-dependent decrease in phosphorylation of p65 subunit | 20515940 | |
| MDA-MB-231 | Function Assay | 50/100 μM | 24 h | increases phosphorylation of JNK in a dose dependent manner | 20515940 | |
| MDA-MB-468 | Function Assay | 50/100 μM | 24 h | increases phosphorylation of JNK in a dose dependent manner | 20515940 | |
| MDA-MB-468 | Function Assay | 100 μM | 24 h | inhibits caspase-3 activation | 20515940 | |
| MDA-MB-468 | Apoptosis Assay | 50/100 μM | 24 h | induces apoptosis | 20515940 | |
| T47D | Function Assay | 100 μM | 48 h | increases the cell number in G1 phase and decreases the cell number in S and G2-M phases | 20515940 | |
| MCF7 | Function Assay | 100 μM | 48 h | increases the cell number in G1 phase and decreases the cell number in S and G2-M phases | 20515940 | |
| MDA-MB-231 | Function Assay | 100 μM | 48 h | increases the cell number in G1 phase and decreases the cell number in S and G2-M phases | 20515940 | |
| MDA-MB-231 | Function Assay | 0-100 μM | 24 h | selectively inhibits Rac1 activation without interfering with the activity of the closely related small GTPase Cdc42 | 20515940 | |
| MDA-MB-231 | Cytotoxicity Assay | 0-100 μM | 48 h | decreases cell viability in a dose dependent manner | 20515940 | |
| MDA-MB-468 | Cytotoxicity Assay | 0-100 μM | 48 h | decreases cell viability in a dose dependent manner | 20515940 | |
| T47D | Cytotoxicity Assay | 0-100 μM | 48 h | decreases cell viability in a dose dependent manner | 20515940 | |
| MCF7 | Cytotoxicity Assay | 0-100 μM | 48 h | decreases cell viability in a dose dependent manner | 20515940 | |
| SKBR3-pMKO.1 | Function Assay | 50 μM | 24 h | inhibits Rac1 activation | 21943825 | |
| SKBR3 | Function Assay | 50 μM | 24 h | inhibits Rac1 activation | 21943825 | |
| NCI-H1703 | Function Assay | 0-500 μM | 24 h | diminishes basal NF-κB activity dose dependently | 22549160 | |
| NCI-H1703 | Function Assay | 100 μg/ml | 24 h | slows progression through the G1 phase of the cell cycle | 22549160 | |
| NCI-H1703 | Growth Inhibition Assay | 0-500 μM | 24 h | inhibits cell growth in a dose dependent manner | 22549160 | |
| T98MG | Function Assay | 50 mM | 24 h | DMSO | enhances the antimigratory effect of erlotinib | 23832120 |
| A172MG | Function Assay | 50 mM | 24 h | DMSO | enhances the antimigratory effect of erlotinib | 23832120 |
| U87MG | Function Assay | 50 mM | 24 h | DMSO | enhances the antimigratory effect of erlotinib | 23832120 |
| PC40 | Cell Viability Assay | 50 mM | 144 h | DMSO | exhibits synergistic antiproliferative effects combined treatment with erlotinib | 23832120 |
| PC38 | Cell Viability Assay | 50 mM | 144 h | DMSO | exhibits synergistic antiproliferative effects combined treatment with erlotinib | 23832120 |
| T98MG | Cell Viability Assay | 50 mM | 144 h | DMSO | exhibits synergistic antiproliferative effects combined treatment with erlotinib | 23832120 |
| A172MG | Cell Viability Assay | 50 mM | 144 h | DMSO | exhibits synergistic antiproliferative effects combined treatment with erlotinib | 23832120 |
| U87MG | Cell Viability Assay | 50 mM | 144 h | DMSO | exhibits synergistic antiproliferative effects combined treatment with erlotinib | 23832120 |
| Ki-67+ CLL | Growth Inhibition Assay | 50 µM | 5 d | decreases the number of Ki-67+ CLL cells | 24501217 | |
| NIH3T3 | Growth Inhibition Assay | 100 μM | 24 h | has no significant impact on cell viability | 25037060 | |
| U2-OS | Function Assay | 100 μM | 24 h | DMSO | induces cell cycle arrest in the G1 phase | 25109327 |
| SW480 | Function Assay | 100 μM | 24 h | DMSO | induces cell cycle arrest in the G1 phase | 25109327 |
| A431 | Function Assay | 100 μM | 24 h | DMSO | induces cell cycle arrest in the G1 phase | 25109327 |
| U2-OS | Growth Inhibition Assay | 100 μM | 24/48/72 h | inhibits cell growth in a time dependent manner | 25109327 | |
| SW480 | Growth Inhibition Assay | 100 μM | 24/48/72 h | inhibits cell growth in a time dependent manner | 25109327 | |
| A431 | Growth Inhibition Assay | 100 μM | 24/48/72 h | inhibits cell growth in a time dependent manner | 25109327 | |
| RBMECs | Function Assay | 100 μM | 30 min | blockes 6Bnz-cAMP-mediated activation of Rac1 in EMAP-II-treated RBMECs | 26358039 | |
| human aortic smooth muscle cells | Function Assay | 50 uM | Inhibition of Rac1 binding to Pak1 in human aortic smooth muscle cells at 50 uM by SDS-PAGE based chemiluminescence | 19527032 | ||
| human aortic smooth muscle cells | Function Assay | 100 μM | Inhibition of Rac1 binding to Pak1 in human aortic smooth muscle cells at 100 uM by SDS-PAGE based chemiluminescence | 19527032 | ||
| Clicca per visualizzare più dati sperimentali sulle linee cellulari | ||||||
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 530.97 | Formula | C24H35N7.3ClH |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 1177865-17-6 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
| Sinonimi | N/A | Smiles | CCN(CC)CCCC(C)NC1=NC(=CC(=N1)NC2=CC3=C(C=C(N=C3C=C2)C)N)C.Cl.Cl.Cl | ||
Solubilità
|
In vitro |
DMSO
: 106 mg/mL
(199.63 mM)
Water : 106 mg/mL Ethanol : 5 mg/mL |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Targets/IC50/Ki |
Rac GTPase
(Cell-free assay) 50 μM
|
|---|---|
| In vitro |
NSC23766 è identificato per inserirsi in un solco superficiale di Rac1 noto per essere critico per la specificazione del GEF. NSC23766 inibisce efficacemente il legame e l'attivazione di Rac1 da parte dei GEF specifici di Rac Trio o Tiam1 in modo dose-dipendente senza interferire con il legame o l'attivazione di Cdc42 o RhoA strettamente correlati da parte dei rispettivi GEF o con l'interazione di Rac1 con BcrGAP o l'effettore PAK1. NSC 23766 è attivo nella regolazione delle funzioni di Rac GTPase sul citoscheletro e su molte funzioni cellulari, inclusi il Cell Cycle, la crescita cellulare, l'adesione, la migrazione e la trascrizione genica. NSC 23766 (50 μM) blocca potentemente l'attivazione di Rac1 indotta dal siero o dal fattore di crescita derivato dalle piastrine e la formazione di lamellipodi senza influenzare l'attività di Cdc42 o RhoA endogeni nelle cellule NIH 3T3. NSC 23766 riduce la crescita delle cellule NIH 3T3 stimolata da Trio o Tiam1, ma non da Vav, Lbc, Intersectin o da un mutante di Rac1 costitutivamente attivo, e sopprime la trasformazione cellulare indotta da Trio, Tiam1 o Ras. NSC23766 inibisce in modo dose-dipendente la proliferazione delle cellule PC-3 e la crescita indipendente dall'ancoraggio. 25 μM di NSC23766 inibiscono l'invasione delle cellule PC-3 attraverso il Matrigel dell'85%. [1] 50 μM di NSC 23766 inibiscono l'attivazione indotta dalla trombina di Rac1 e Rac2 nelle piastrine umane, così come l'aggregazione piastrinica. NSC23766 previene la produzione di Aβ40 e Aβ42 nelle cellule swAPP-HEK293 senza influenzare Notch e sAPPα. NSC23766 previene l'attività della γ-secretasi nella cellula, ma non agisce come un inibitore diretto della γ-secretasi. NSC23766 riduce in modo dose-dipendente i livelli di Aβ40 secreto e intracellulare con un IC50 di 48,94 μM. 50 μM di NSC 23766 inibiscono il rilascio di Aβ42 del 57,97 %. NSC23766 regola l'espressione della ossido nitrico sintasi endoteliale e la funzione endoteliale. 100 μM di NSC23766 reprimono l'attività del promotore di eNOS del 60% nelle EC aortiche bovine e del 30% al 35% nelle cellule bEND.3. L'inibizione di Rac1 con NSC23766 destabilizza l'mRNA di eNOS e ne accorcia l'emivita a 17 ore. NSC23766 attenua in modo dose-dipendente il rilassamento indotto da ACh degli anelli aortici di topi wild-type. NSC23766 inibisce la crescita cellulare e induce l'apoptosi. NSC23766 diminuisce la vitalità delle cellule MDA-MB-468 e MDA-MB-231 in modo dose-dipendente con un IC50 di ~10 μM, che non è correlato allo stato del recettore degli estrogeni (ER), del recettore del progesterone (PR), di Her2 e della mutazione p53. NSC23766 ha scarso effetto sulla sopravvivenza delle cellule epiteliali mammarie normali MCF12A. Dopo 24 ore di esposizione a NSC 23766, le cellule MDA-MB-231 hanno mostrato un aumento dal 41% al 65% nella fase G1 e una concomitante diminuzione nelle fasi S e G2-M. 100 μM di NSC23766 inducono un aumento di sei volte delle MDA-MB-468 apoptotiche. L'inibizione di NSC23766 sull'arresto del Cell Cycle o sull'apoptosi nelle cellule di cancro al seno è mediata dalla down-regolazione della ciclina D1, della survivina e dell'inibitore dell'apoptosi legato al cromosoma X. |
| Saggio chinasico |
Saggio di attività di Rho GTPase
|
|
Le cellule vengono coltivate in fase logaritmica in una piastra da 10 cm e vengono private di siero in un terreno con 0,5% di siero o indicato altrimenti per 24 ore prima della lisi in un tampone contenente 20 mM Tris HCl (pH 7,6), 100 mM NaCl, 10 mM MgCl2, 1% Nonidet P-40, 10% glicerolo e una miscela di inibitori di proteasi 1×. I lisati vengono chiarificati, le concentrazioni proteiche vengono normalizzate e il Rac1 legato al GTP nei lisati viene misurato mediante un saggio di pull-down del dominio effettore. Per il saggio di pull-down di His6-PAK1 PBD, i lisati cellulari vengono incubati con il dominio His6-PAK1 PBD immobilizzato su Ni2+-agarosio (~1 μg ciascuno) purificato da E. coli per 30 min. I coprecipitati di Ni2+-agarosio vengono lavati due volte nel tampone di lavaggio e analizzati mediante immunoblotting con anticorpo monoclonale anti-Rac1.
|
|
| In vivo |
NSC23766 induce la mobilizzazione delle cellule staminali/progenitrici ematopoietiche. La somministrazione intraperitoneale di NSC23766 (2,5 mg/kg) nel ceppo di topo C57Bl/6 «scarsamente mobilizzante» porta a un aumento di due volte delle cellule staminali/progenitrici ematopoietiche circolanti 6 ore dopo l'iniezione. NSC23766 allevia il danno polmonare acuto indotto da lipopolisaccaridi nei topi. Il trattamento con NSC23766 a 1 o 3 mg/kg non solo riduce l'infiltrazione delle cellule infiammatorie e le attività della MPO, ma inibisce anche l'espressione di mRNA dei mediatori pro-infiammatori, il fattore di necrosi tumorale-α e l'interleuchina-1β. NSC23766 riduce anche l'accumulo di Evans Blue e albumina nei polmoni sottoposti a LPS. |
Riferimenti |
|
Applicazioni
| Metodi | Biomarcatori | Immagini | PMID |
|---|---|---|---|
| Western blot | pCREB / CREB OCT4 / SOX2 / Nanog active Rac1 / Rac1 |
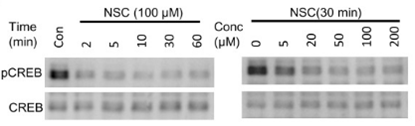
|
25319697 |
| Immunofluorescence | IP3K-A / F-actin BART / Rac1 |
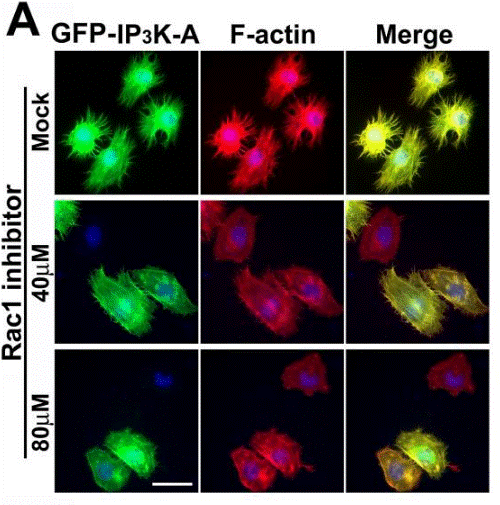
|
19890013 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
