solo per uso di ricerca
Butein EGFR inibitore
N. Cat.S8036
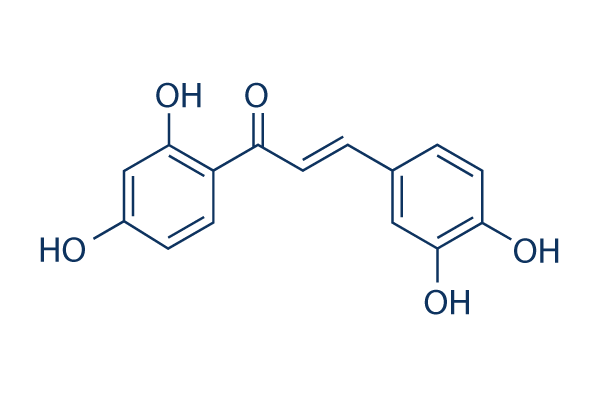
Struttura chimica
Peso molecolare: 272.25
Controllo Qualità
- Citato in Nature Medicine per la sua qualità superiore
- COA
- NMR
- SDS
- Scheda tecnica
| Target correlati | VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Altro EGFR Inibitori | Lazertinib (YH25448) Icotinib Hydrochloride Sunvozertinib AG-490 AG-1478 Canertinib (CI-1033) WZ4002 Rociletinib (CO-1686) Poziotinib (NOV120101, HM781-36B) Genistein |
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 272.25 | Formula | C15H12O5 |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 487-52-5 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
| Sinonimi | N/A | Smiles | C1=CC(=C(C=C1C=CC(=O)C2=C(C=C(C=C2)O)O)O)O | ||
Solubilità
|
In vitro |
DMSO
: 55 mg/mL
(202.02 mM)
Ethanol : 55 mg/mL Water : Insoluble |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Targets/IC50/Ki |
EGFR
|
|---|---|
| In vitro |
Butein inibisce il livello di autofosfotirosina del recettore EGF stimolato dal fattore di crescita epidermico (EGF) nelle cellule HepG2, e inibisce anche le attività di Protein Tyrosine Kinase tirosina-specifiche del recettore EGF e di p60c-src con una IC50 di 65 μM in vitro. L'inibizione è competitiva con l'ATP e non competitiva con l'accettore di fosfato, poli (Glu, Ala, Tyr) 6:3:1 per la tirosina chinasi del recettore EGF. Al contrario, questo composto non inibisce significativamente le attività delle Protein Tyrosine Kinase serina- e treonina-specifiche come PKC o PKA. Questa sostanza chimica inibisce il Nuclear Factor (NF)-κB e l'espressione genica regolata da NF-κB attraverso l'inibizione diretta di IκBα Kinase β sul residuo Cisteina 179. Esso (10 μM) inibisce oltre il 90% dell'espressione di iNOS e COX-2, così come la produzione di nitriti e TNF-α nelle cellule RAW 264.7 stimolate da LPS. Questo composto (10 μM) inibisce l'attività di legame al DNA di NF-κB indotta da LPS, che è mediata attraverso l'inibizione della degradazione del fattore inibitorio-κB e la fosforilazione della chinasi MAP Erk1/2, oltre ad aumentare il legame del recettore integrinico osteopontina a vb3. Il trattamento (20 μM) induce cambiamenti morfologici delle cellule di cancro alla vescica BLS(M) da una morfologia allungata a cellule arrotondate simili a epiteliali, accompagnati dalla downregulation della vimentina e dall'acquisizione di E-caderina rispetto alle cellule di controllo non trattate, indicando l'inversione del fenotipo mesenchimale. Questa sostanza chimica (20 μM) sopprime la motilità e la capacità di invasione delle cellule BLS(M) e inverte il fenotipo simile a EMT indotto dal TNF-α, attraverso le vie di segnalazione ERK1/2 e NF-κB. Inibisce l'attivazione costitutiva di STAT3 nelle cellule HepG2 in modo dose-dipendente, con massima inibizione a 50 μM, mediata dall'inibizione dell'attivazione delle chinasi a monte c-Src e Janus-activated kinase2. Questo composto (50 μM) potrebbe anche inibire completamente la fosforilazione di STAT3 indotta da IL-6 nelle cellule SNU-387. Downregola l'espressione di ciclina D1, Bcl-2, Bcl-xL, survivina e VEGF, marcatori dell'attivazione di STAT3. Questa sostanza chimica (50 μM) aumenta significativamente gli effetti apoptotici della doxorubicina dal 18% al 55% e del paclitaxel dal 15% al 42%. È un potente antiossidante contro la perossidazione lipidica e delle LDL. Questo composto inibisce la perossidazione lipidica indotta dal ferro nell'omogenato di cervello di ratto con una IC50 di 3,3 μM. È potente come l'α-tocoferolo nel ridurre il radicale libero stabile difenil-2-picrilidrazile (DPPH) con una IC0,2 di 9,2 μM. Questa sostanza chimica inibisce anche l'attività della xantina ossidasi con una IC50 di 5,9 μM. Scavenga il radicale perossilico derivato dal 2,2-azobis(2-amidinopropano) dicloridrato (AAPH) in fase acquosa. Inoltre, questo composto inibisce l'ossidazione catalizzata dal rame delle lipoproteine a bassa densità (LDL) umane in modo concentrazione-dipendente. È un chelante degli ioni ferrosi e rameici.
|
| In vivo |
Butein a 2 mg/kg induce una significativa inibizione della crescita del tumore epatocellulare rispetto ai controlli trattati con olio di mais. All'autopsia al giorno 22 dopo il trattamento iniziale, si osserva una diminuzione di oltre 2 volte nella crescita tumorale in questo gruppo trattato con il composto (carico tumorale relativo medio, 3,90) rispetto al gruppo di controllo (8,46), associata a una ridotta p-STAT3 costitutiva (9% vs 81% del gruppo veicolo), a livelli di Bcl-2 (26% vs 96% del gruppo veicolo) e a un aumentato livello di caspasi-3 (98% vs 21% del gruppo veicolo) nei tessuti tumorali di HCC. Questo composto mostra attività antifibrogenica. Esso (25 mg/kg/die) riduce l'attivazione sierica di AST e ALT rispettivamente al 35% e 69% dei livelli nei ratti di controllo indotti da CCl4. Questa sostanza chimica (25 mg/kg/die) riduce i contenuti di idrossiprolina e la concentrazione di TBAR4 nel fegato rispettivamente al 54% e 54%. L'espressione del collagene α1(I) e del TIMP-1 nei ratti trattati con questo composto è del 28% e 20,3% rispetto ai valori per il rispettivo controllo trattato con CCl4.
|
Riferimenti |
|
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
