solo per uso di ricerca
Cinnamaldehyde TRP Channel agonista
N. Cat.S3763
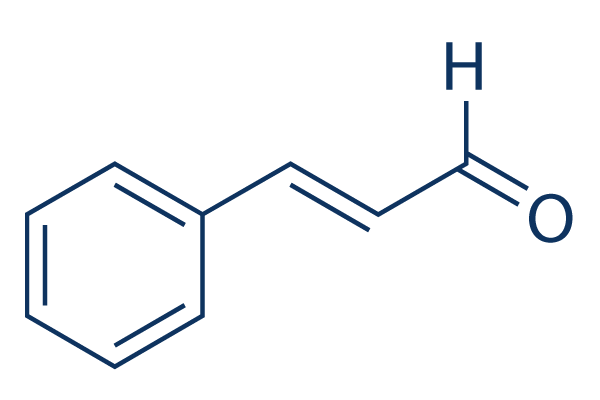
Struttura chimica
Peso molecolare: 132.16
Controllo Qualità
- Citato in Nature Medicine per la sua qualità superiore
- COA
- NMR
- SDS
- Scheda tecnica
| Target correlati | CFTR CRM1 CD markers AChR Calcium Channel Sodium Channel Potassium Channel GABA Receptor ATPase GluR |
|---|---|
| Altro TRP Channel Inibitori | 2-APB (2-Aminoethyl Diphenylborinate) SKF96365 AMG-517 GSK2193874 GSK1016790A HC-030031 Capsazepine EIPA (L593754) SB705498 HC-067047 |
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 132.16 | Formula | C9H8O |
Conservazione (Dalla data di ricezione) | 2 years -20°C liquid |
|---|---|---|---|---|---|
| N. CAS | 14371-10-9 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
Solubilità
|
In vitro |
|
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Targets/IC50/Ki |
TRPA1
|
|---|---|
| In vitro |
Cinnamaldehyde (40 μM) potrebbe aumentare l'espressione della lipasi sensibile agli ormoni (HSL) e sopprimere l'espressione di perilipina e glicerolo-3-fosfato deidrogenasi, oltre a ridurre l'espressione dei geni adipocitari del recettore attivato dai proliferatori perossisomiali (PPAR)-γ e della proteina legante CCAAT/enhancer-α (CEBP-α) nei pre-adipociti 3T3-L1. Aumenta anche l'espressione di PPARδ e PPARγ, così come dei suoi geni bersaglio come aP2 e CD36 negli adipociti differenziati 3T3-L1. Il trattamento con questo composto aumenta l'espressione di GLUT4 attivando il coattivatore 1α del recettore γ attivato dai proliferatori perossisomiali (PGC-1α) e innescando il suo effettore a valle, i fattori di miglioramento dei miociti 2 (MEF2) nelle cellule C2C12. Il suo trattamento regola il metabolismo ossidativo aumentando le espressioni della 5'-adenosina monofosfato-chinasi attivata (AMPK), della deacetilasi NAD+-dipendente sirtuina 1, di PGC-1α e del citocromo C, oltre a migliorare l'espressione di PPARα e PPARβ/δ, il che contribuisce alla biogenesi mitocondriale. Tuttavia, è dimostrato che inibisce il metabolismo mitocondriale riducendo il metabolismo ossidativo basale e indotto chimicamente dei miotubi nelle cellule C2C12. Questa sostanza chimica esercita effetti citotossici sulle cellule di leucemia umana K562 inducendo apoptosi e sinergizzando la citotossicità delle cellule CIK contro le cellule K562.
|
| In vivo |
Cinnamaldehyde mostra effetti di abbassamento dei glucolipidi negli animali diabetici aumentando l'assorbimento del glucosio e migliorando la sensibilità all'insulina nei tessuti adiposi e muscolari scheletrici, migliorando la sintesi del glicogeno nel fegato, ripristinando la disfunzione delle isole pancreatiche, rallentando i tassi di svuotamento gastrico e migliorando i disturbi renali e cerebrali diabetici. Questo composto esercita questi effetti attraverso la sua azione su molteplici vie di segnalazione, inclusi PPAR, AMPK, PI3K/IRS-1, RBP4-GLUT4 e ERK/JNK/p38MAPK, TRPA1-ghrelin e le vie Nrf2. Inoltre, questo composto sembra regolare le attività di PTP1B e α-amilasi. La somministrazione orale di questa sostanza chimica, che va da 20 mg/kg a 40 mg/kg al giorno per una durata compresa tra 21 e 60 giorni, porta a un miglioramento significativo dei livelli di glucosio nel sangue e di emoglobina glicosilata (HbA1C), nonché della sensibilità all'insulina nei ratti diabetici indotti da STZ. Non è stabile nell'organismo, con la possibilità di metabolizzare in acido cinnamico e trasformarsi in alcol cinnamico. Dosi eccessive di questo composto possono generare una risposta tossica. Nell'uomo, il 3% di questa sostanza può causare irritazione cutanea. È dimostrato che diminuisce l'IL-1β sierica e inibisce l'espressione genica infiammatoria (COX-2, MCP-1, TNF-α e IL-6) nel WAT di topi albini svizzeri maschi e C57BLKS db/db insultati da HFD, mentre un'aumentata espressione di Cpt1a protegge contro il rilascio di adipochine pro-infiammatorie e promuove l'ossidazione degli acidi grassi, il che contribuisce a un miglioramento della resistenza all'insulina.
|
Riferimenti |
|
Informazioni sullo studio clinico
(dati da https://clinicaltrials.gov, aggiornato il 2024-05-22)
| Numero NCT | Reclutamento | Condizioni | Sponsor/Collaboratori | Data di inizio | Fasi |
|---|---|---|---|---|---|
| NCT05654298 | Completed | Migraine |
Universitaire Ziekenhuizen KU Leuven |
March 15 2022 | Not Applicable |
| NCT04183283 | Completed | Healthy |
Eli Lilly and Company |
December 12 2019 | Phase 1 |
| NCT04415892 | Unknown status | Chemotherapy-induced Peripheral Neuropathy |
Universitaire Ziekenhuizen KU Leuven |
October 1 2019 | Not Applicable |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
