solo per uso di ricerca
Diazoxide ADC Cytotoxin inibitore
N. Cat.S4630
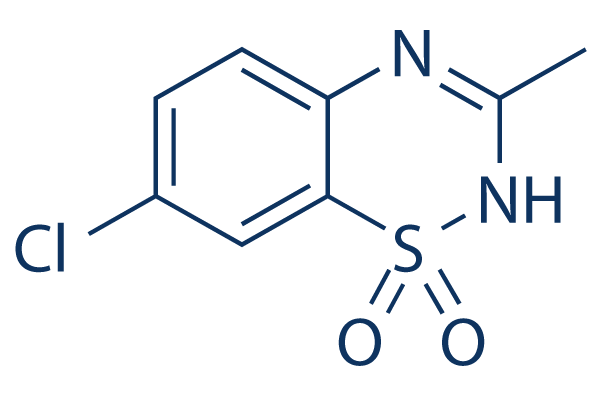
Struttura chimica
Peso molecolare: 230.67
Controllo Qualità
| Target correlati | CFTR CRM1 CD markers AChR Calcium Channel Sodium Channel Potassium Channel GABA Receptor TRP Channel ATPase |
|---|---|
| Altro ADC Cytotoxin Inibitori | Triptolide SN-38 Luteolin (+)-Bicuculline Rutin Artemisinin BHQ Pinocembrin Harmine hydrochloride Luteoloside |
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 230.67 | Formula | C8H7ClN2O2S |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 364-98-7 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
| Sinonimi | Sch-6783, SRG-95213 | Smiles | CC1=NS(=O)(=O)C2=C(N1)C=CC(=C2)Cl | ||
Solubilità
|
In vitro |
DMSO
: 46 mg/mL
(199.41 mM)
Water : Insoluble Ethanol : Insoluble |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Targets/IC50/Ki |
KATP channels
|
|---|---|
| In vitro |
Diazoxide inibisce l'attività infiammatoria microgliale. Il trattamento con questo composto inibisce parzialmente il pattern infiammatorio indotto da LPS/IFN-γ nelle cellule microgliali, inducendo una diminuzione della produzione di NO che potrebbe essere dovuta alla diminuita espressione di iNOS rilevata. Non ha alcun effetto sulla fagocitosi microgliale.
|
| In vivo |
Diazoxide è benefico per il miglioramento delle funzioni cognitive, la riduzione dell'ansia, la diminuzione dell'accumulo di oligomeri di beta-amiloide e l'iperfosforilazione delle proteine tau. Questo composto può anche esercitare effetti neuroprotettivi indipendentemente dall'attivazione dei canali K+ diminuendo l'eccitabilità neuronale e l'attivazione dei recettori N-metil-D-aspartato (NMDA) o aumentando le correnti attraverso i recettori dell'acido α-amino-3-idrossi-5-metil-4-isoxazolepropionico (AMPA). Gli animali trattati con questa sostanza chimica mostrano una diminuzione della gravità della malattia pochi giorni dopo l'osservazione dei primi segni clinici, corrispondenti alla fase infiammatoria acuta della malattia. La somministrazione orale giornaliera di questo composto in topi EAE durante la fase effettore della malattia riduce la gravità dei segni clinici senza alcun apparente effetto avverso. Diminuisce la demielinizzazione e la perdita assonale, riduce il danno tissutale, inibisce l'attivazione microgliale/macrofagica e astrocitaria e preserva l'integrità neuronale. Non si osservano effetti sul numero di linfociti B e T che infiltrano il midollo spinale.
|
Riferimenti |
|
Informazioni sullo studio clinico
(dati da https://clinicaltrials.gov, aggiornato il 2024-05-22)
| Numero NCT | Reclutamento | Condizioni | Sponsor/Collaboratori | Data di inizio | Fasi |
|---|---|---|---|---|---|
| NCT03941236 | Active not recruiting | Congenital Hyperinsulinism |
Zealand Pharma |
May 1 2019 | Phase 3 |
| NCT00901823 | Withdrawn | Hypertriglyceridemia |
Essentialis Inc. |
March 2011 | Phase 1 |
| NCT00696475 | Completed | Hypertriglyceridemia |
Essentialis Inc.|Medpace Inc. |
June 2008 | Phase 2 |
| NCT00688857 | Completed | Hypertriglyceridemia |
Essentialis Inc.|Cetero Research San Antonio |
May 2008 | Phase 1 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
