solo per uso di ricerca
Fluvastatin Sodium HMG-CoA Reductase inibitore
N. Cat.S1909
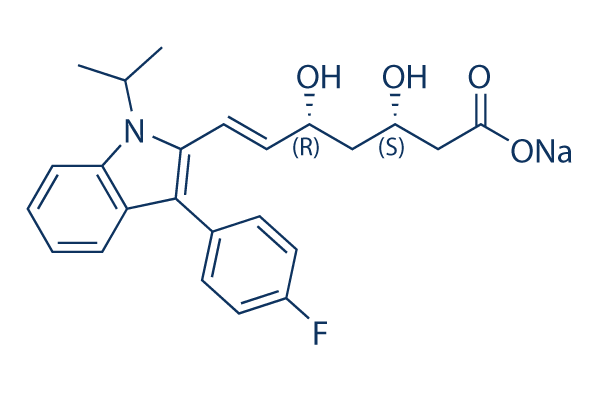
Struttura chimica
Peso molecolare: 433.45
Controllo Qualità
| Target correlati | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Altro HMG-CoA Reductase Inibitori | Mevastatin SR-12813 Clinofibrate Dihydrolanosterol 7-ketocholesterol Cerivastatin sodium |
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 433.45 | Formula | C24H25FNNaO4 |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 93957-55-2 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
| Sinonimi | XU-62-320 Sodium | Smiles | CC(C)N1C2=CC=CC=C2C(=C1C=CC(CC(CC(=O)[O-])O)O)C3=CC=C(C=C3)F.[Na+] | ||
Solubilità
|
In vitro |
DMSO
: 87 mg/mL
(200.71 mM)
Water : 18 mg/mL Ethanol : Insoluble |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Caratteristiche |
The order of magnitude of inhibition of each drug on the peroxidation was butylated hydroxytoluene > fluvastatin ≥ probucol ≥ pravastatin.
|
|---|---|
| Targets/IC50/Ki |
HMG-CoA reductase
(Cell-free assay) 8 nM
|
| In vitro |
Fluvastatin inibisce marcatamente la formazione di sostanze reattive all'acido tiobarbiturico nella perossidazione di liposomi supportata da ferro (II) con un IC50 di 12 μM. Fluvastatin, a concentrazioni da 1 μM a 100 μM, inibisce la perossidazione di liposomi mediata da radicali perossidici indotta da generatori di radicali idrosolubili e liposolubili, rispettivamente 2,2'-azobis (2-amidinopropano) dicloridrato e 2,2'-azobis (2,4-dimetilvaleronitrile). Fluvastatin (4 mM) e i suoi metaboliti mostrano attività di scavenging dell'anione superossido nel sistema ipoxantina-xantina ossidasi e un forte effetto di scavenging sul radicale idrossilico prodotto dalla reazione di Fenton. Fluvastatin (8 μM) e i suoi metaboliti mostrano effetti protettivi sul danno al DNA potenti quanto gli antiossidanti di riferimento, acido ascorbico, trolox e probucol nelle cellule CHL/IU. Fluvastatin (100 nM) mostra una diminuzione dose-dipendente della formazione di anione superossido attivata da Ang II nelle cellule muscolari lisce aortiche umane (hASMC). |
| In vivo |
La Fluvastatin (10 mg/kg/die) determina una diminuzione dei lipidi sierici in conigli alimentati con una dieta contenente 1,5% di colesterolo. La Fluvastatin (10 mg/kg/die) riduce significativamente l'ACE tissutale nelle aorte di conigli alimentati con una dieta contenente 1,5% di colesterolo. La Fluvastatin (10 mg/kg/die) inverte significativamente la soppressione del rilassamento indotto da ACh in conigli alimentati con una dieta contenente 1,5% di colesterolo. |
Riferimenti |
|
Applicazioni
| Metodi | Biomarcatori | Immagini | PMID |
|---|---|---|---|
| Growth inhibition assay | Cell viability |
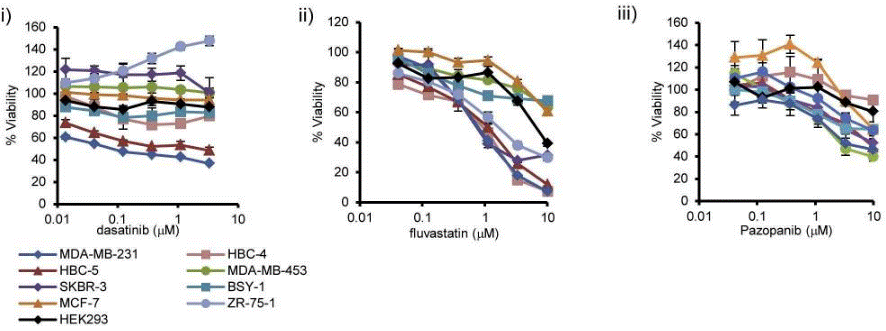
|
26199863 |
| Western blot | p53 / p21 / Cyclin D1 / ATF3 / H3P / PARP / Cleaved PARP / γ-H2AX YAP1 / TAZ / RHAMM |
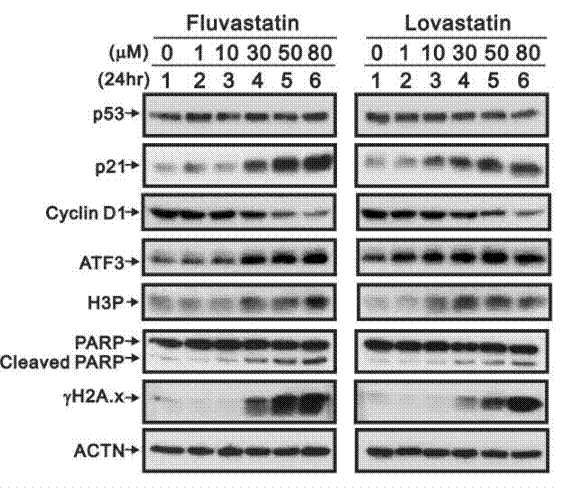
|
30939155 |
| Immunofluorescence | YAP1 |
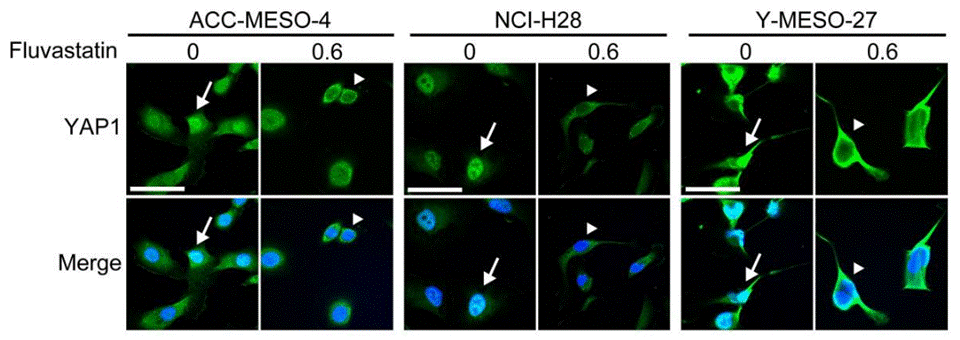
|
29212185 |
Informazioni sullo studio clinico
(dati da https://clinicaltrials.gov, aggiornato il 2024-05-22)
| Numero NCT | Reclutamento | Condizioni | Sponsor/Collaboratori | Data di inizio | Fasi |
|---|---|---|---|---|---|
| NCT02115074 | Completed | Glioma |
Centre Oscar Lambret|Anticancer Fund Belgium |
June 2014 | Phase 1 |
| NCT01524601 | Completed | Disorder Related to Renal Transplantation|Hypercholesterolemia |
University of Oslo School of Pharmacy|Oslo University Hospital |
February 2012 | Phase 4 |
| NCT00814606 | Withdrawn | Hepatitis C|Hepatitis C Virus |
University of Chicago |
February 2010 | Phase 2 |
| NCT00752843 | Completed | Healthy Subjects |
Corcept Therapeutics |
September 2008 | Phase 1 |
| NCT00674297 | Completed | Antiphospholipid Syndrome |
Hospital for Special Surgery New York|University of Texas |
May 2008 | Phase 2 |
| NCT00404287 | Terminated | Aortic Valve Stenosis |
AORTICA Group |
October 1 2006 | Phase 4 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
