solo per uso di ricerca
Azilsartan Angiotensin Receptor antagonista
N. Cat.S3046
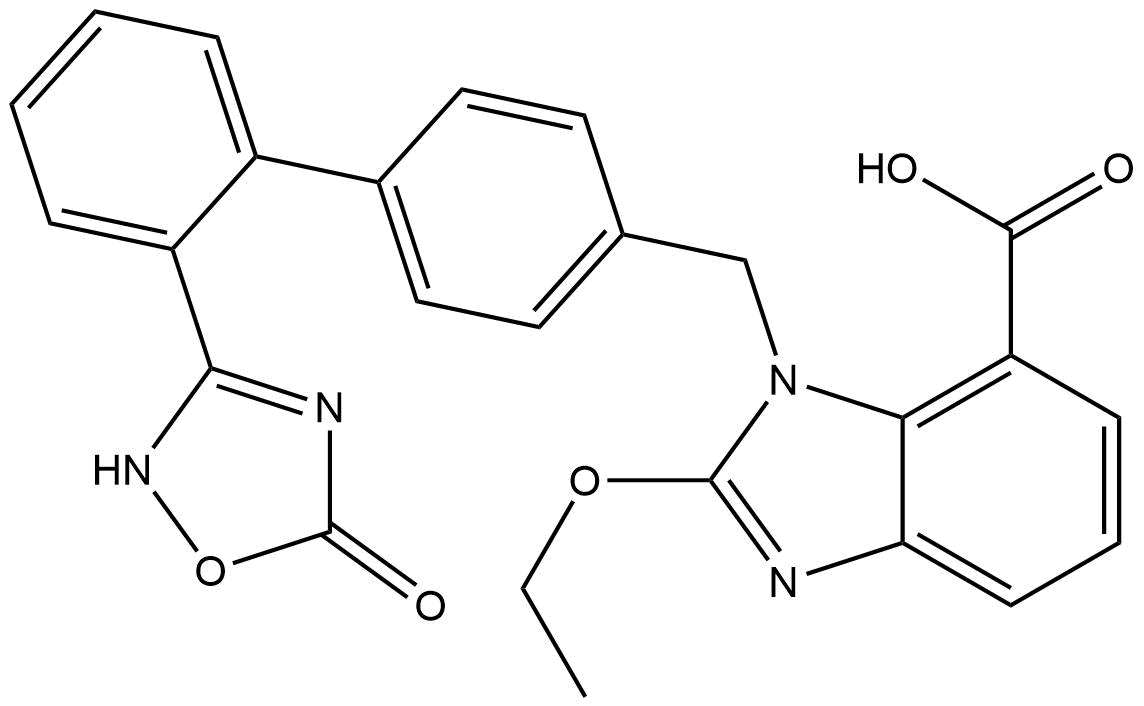
Struttura chimica
Peso molecolare: 456.45
Controllo Qualità
- Citato in Nature Medicine per la sua qualità superiore
- COA
- NMR
- HPLC
- SDS
- Scheda tecnica
| Target correlati | CXCR Hedgehog/Smoothened PKA Adrenergic Receptor AChR 5-HT Receptor Histamine Receptor Dopamine Receptor Ras KRas |
|---|---|
| Altro Angiotensin Receptor Inibitori | PD123319 ML221 A-779 Fimasartan Olodanrigan (EMA401) Buloxibutid AVE 0991 |
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 456.45 | Formula | C25H20N4O5 |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 147403-03-0 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
| Sinonimi | TAK-536 | Smiles | CCOC1=NC2=CC=CC(=C2N1CC3=CC=C(C=C3)C4=CC=CC=C4C5=NOC(=O)N5)C(=O)O | ||
Solubilità
|
In vitro |
DMSO
: 91 mg/mL
(199.36 mM)
Water : Insoluble Ethanol : Insoluble |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Caratteristiche |
A potent, orally active and specific AII receptor antagonist.
|
|---|---|
| Targets/IC50/Ki |
AT1 receptor
2.6 nM
|
| In vitro |
Azilsartan inibisce il legame specifico di 125I-Sar1-Ile8-AII ai recettori umani dell'angiotensina di tipo 1. Questo composto inibisce anche l'accumulo di inositolo 1-fosfato (IP1) indotto da AII nell'analisi basata su cellule con un valore di IC50 di 9,2 nM. In strisce aortiche isolate di coniglio, riduce la risposta contrattile massima ad AII con un valore di pD'2 di 9,9. Gli effetti inibitori di questa sostanza chimica sulle risposte contrattili indotte da AII persistono dopo il lavaggio delle strisce. Sopprime l'aumento del livello di glucosio plasmatico nel test di tolleranza al glucosio orale (OGTT) senza modifiche significative nella concentrazione di insulina e migliora la sensibilità all'insulina. Nel muscolo scheletrico, questo agente diminuisce l'espressione di TNF-α a dosi dello 0,001%. Nel tessuto adiposo, riduce l'espressione di TNF-α ma aumenta l'espressione di adiponectina, PPARγ, C/EBα e aP2. In preadipociti 3T3-L1 coltivati, questo composto migliora l'adipogenesi ed esercita effetti maggiori rispetto al valsartan sull'espressione dei geni che codificano il recettore attivato dai proliferatori perossisomiali-α (PPARα), PPARδ, leptina, adipsina e adiponectina. Inoltre, inibisce potentemente la proliferazione delle cellule vascolari in assenza di angiotensina II supplementata esogenamente.
|
| Saggio chinasico |
Studi di legame con radioligandi sui recettori AT1 umani
|
|
Un saggio di legame con radioligandi viene eseguito utilizzando micropiastre rivestite di recettori AT1 umani contenenti da 4,4 a 6,2 fmol di recettori/pozzetto (10 μg di proteina di membrana/pozzetto). I pozzetti rivestiti di membrana vengono incubati con 45 μL di tampone di saggio (50 mM Tris-HCl, 5 mM MgCl2, 1 mM EDTA e 0,005% CHAPS, pH 7,4) contenente varie concentrazioni di Azilsartan a temperatura ambiente. Dopo 90 minuti, 5 μL di 125I-Sar1-Ile8-AII (concentrazione finale 0,6 nM) disciolti nel tampone di saggio vengono aggiunti ai pozzetti e la piastra viene incubata per 5 ore. Ad ogni passaggio, la piastra viene brevemente e delicatamente agitata su un agitatore per piastre. Negli esperimenti di lavaggio, le membrane vengono incubate con questo composto per 90 minuti, quindi immediatamente lavate due volte con 200 μL/pozzetto di tampone di saggio per rimuovere i composti non legati e ulteriormente incubate per 5 ore con 125I-Sar1-Ile8-AII. La radioattività legata alla membrana viene contata utilizzando un TopCount Microplate Scintillation and Luminescence Counter. Negli esperimenti per stimare la velocità di dissociazione di questa sostanza chimica dai recettori AT1, le membrane vengono incubate per 90 minuti con questo composto a una concentrazione di 30 nM. Questo composto inibisce il legame specifico di 125I-Sar1-Ile8-AII agli AT1 umani di circa il 90%. Le membrane vengono quindi immediatamente lavate due volte con 200 μL/pozzetto di tampone di saggio e ulteriormente incubate con 125I-Sar1-Ile8-AII per 240 minuti. La radioattività legata alla membrana viene contata utilizzando il TopCount Microplate Scintillation and Luminescence Counter a 30 minuti, 60 minuti, 90 minuti, 120 minuti, 150 minuti, 180 minuti o 240 minuti. Il legame non specifico di 125I-Sar1-Ile8-AII viene stimato in presenza di 10 μM di AII non marcato. AII non marcato viene aggiunto nuovamente dopo il lavaggio per l'esperimento di lavaggio. Il legame specifico è definito come il legame totale meno il legame non specifico.
|
|
| In vivo |
Nei ratti Koletsky, il trattamento con Azilsartan abbassa la pressione sanguigna, la concentrazione basale di insulina plasmatica e l'indice di valutazione del modello di omeostasi della resistenza all'insulina, e ha inibito l'eccessivo aumento delle concentrazioni plasmatiche di glucosio e insulina durante il test di tolleranza al glucosio orale. Questo composto downregola l'espressione dell'11β-idrossisteroide deidrogenasi di tipo 1.
|
Riferimenti |
|
Informazioni sullo studio clinico
(dati da https://clinicaltrials.gov, aggiornato il 2024-05-22)
| Numero NCT | Reclutamento | Condizioni | Sponsor/Collaboratori | Data di inizio | Fasi |
|---|---|---|---|---|---|
| NCT04668157 | Completed | Hypertension |
Takeda |
May 17 2021 | Phase 3 |
| NCT03434977 | Completed | Healthy Volunteers |
Takeda |
February 14 2018 | Phase 1 |
| NCT03042299 | Completed | Japanese Healthy Adult Male Participants |
Takeda |
February 10 2017 | Phase 1 |
| NCT02791438 | Completed | Pediatric Hypertension |
Takeda |
August 18 2016 | Phase 3 |
| NCT02541669 | Completed | Healthy Volunteer |
Takeda |
November 20 2015 | Phase 1 |
| NCT02451150 | Completed | Pediatric Hypertension |
Takeda |
August 2015 | Phase 3 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
