solo per uso di ricerca
Rivaroxaban Factor Xa inibitore
N. Cat.S3002
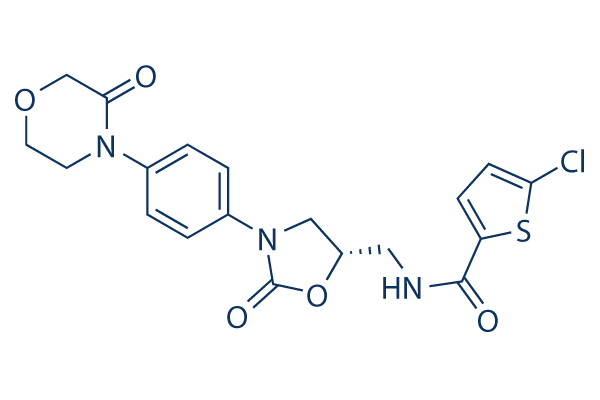
Struttura chimica
Peso molecolare: 435.88
Controllo Qualità
| Target correlati | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Altro Factor Xa Inibitori | Asundexian |
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 435.88 | Formula | C19H18ClN3O5S |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 366789-02-8 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
| Sinonimi | BAY 59-7939 | Smiles | C1COCC(=O)N1C2=CC=C(C=C2)N3CC(OC3=O)CNC(=O)C4=CC=C(S4)Cl | ||
Solubilità
|
In vitro |
DMSO
: 87 mg/mL
(199.59 mM)
Water : Insoluble Ethanol : Insoluble |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Targets/IC50/Ki |
Factor Xa
(Cell-free assay) 0.7 nM
Prothrombinase
(Cell-free assay) 2.1 nM
|
|---|---|
| In vitro |
Rivaroxaban è un inibitore orale diretto del Factor Xa (FXa), in fase di sviluppo per la prevenzione e il trattamento della trombosi arteriosa e venosa con un Ki di 0,4 nM. Questo composto inibisce anche l'attività protrombinasica con IC50 di 2,1 nM. Mostra anche un'affinità simile per il FXa umano e di coniglio purificati (IC50 0,7 nM e 0,8 nM, rispettivamente), ma una potenza minore contro il FXa di ratto purificato (IC50 3,4 nM). Il FXa umano e di coniglio endogeno nel plasma è inibito in misura simile da questa sostanza chimica (IC50 21 nM e 21 nM, rispettivamente), mentre sono necessarie concentrazioni 14 volte superiori nel plasma di ratto (IC50 290 nM). Esibisce alta permeabilità e trasporto polarizzato attraverso le cellule Caco-2 come substrato della P-gp, ma non mostra alcun effetto inibitorio sul trasporto di farmaci mediato dalla P-gp fino a concentrazioni di 100 μM in vitro.
|
| Saggio chinasico |
Attività del Factor Xa
|
|
L'attività di Rivaroxaban contro le serina proteasi purificate viene misurata utilizzando substrati cromogenici o fluorogenici in micropiastre a 96 pozzetti. Gli enzimi vengono incubati con questo composto o il suo solvente, dimetilsolfossido (DMSO), per 10 minuti. Le reazioni vengono avviate mediante l'aggiunta del substrato e il colore o la fluorescenza viene monitorata continuamente a 405 nm utilizzando un lettore Spectra Rainbow Thermo, o a 630/465 nm utilizzando uno SPECTRAfluor plus, rispettivamente, per 20 minuti. L'attività enzimatica viene analizzata nei seguenti tamponi (concentrazioni finali): FXa umano (0,5 nM), FXa di coniglio (2 nM), FXa di ratto (10 nM) o urochinasi (4 nM) in tampone Tris–HCl 50 mM pH 8,3, 150 mM NaCl e 0,1% di albumina di siero bovino (BSA); Pefachrome FXa (50–800 μM) o cromozima U (250 μM) con trombina (0,69 nM), tripsina (2,2 nM) o plasmina (3,2 nM) in 0,1 μM Tris–HCl, pH 8,0, e 20 mM CaCl2; cromozima TH (200 μM), cromozima plasmina (500 μM) o cromozima tripsina (500 μM) con FXIa (1 nM) o APC (10 nM) in tampone fosfato 50 mM, pH 7,4, 150 mM NaCl; e S 2366 (150 o 500 μM) con FVIIa (1 nM) e fattore tissutale (3 nM) in tampone Tris–HCl 50 mM, pH 8,0, 100 mM NaCl, 5 mM CaCl2 e 0,3% BSA, H-D-Phe-Pro-Arg-6-amino-1-naftalene-benzil-sulfonamide-H2O (100 μM) e misurata per 3 ore. Il saggio FIXaβ/FX, comprendente FIXaβ (8,8 nM) e FX (9,5 nM) in tampone Tris–HCl 50 mM, pH 7,4, 100 mM NaCl, 5 mM CaCl2 e 0,1% BSA, viene avviato con l'aggiunta di I-1100 (50 μM) e misurato per 60 minuti. La costante inibitoria (Ki) contro il FXa viene calcolata secondo l'equazione di Cheng–Prusoff. L'IC50 è la quantità di inibitore necessaria per diminuire la velocità iniziale del controllo del 50%.
|
|
| In vivo |
Rivaroxaban riduce la trombosi venosa in modo dose-dipendente (ED50 0,1 mg/kg i.v.) in un modello di stasi venosa nel ratto. Questo composto riduce la formazione di trombi arteriosi in uno shunt artero-venoso (AV) in ratti (ED50 5,0 mg/kg p.o.) e conigli (ED50 0,6 mg/kg p.o.). La farmacocinetica plasmatica di questa sostanza chimica è lineare nell'intervallo di dosi investigato (1-10 mg/kg nei ratti, 0,3-3 mg/kg nei cani). La clearance plasmatica è bassa: 0,4 L/kg/h nei ratti e 0,3 L/kg/h nei cani; il volume di distribuzione (V(ss)) è moderato: 0,3 L/kg nei ratti e 0,4 L/kg nei cani. L'emivita di eliminazione dopo somministrazione orale è breve in entrambe le specie (0,9-2,3 ore).
|
Riferimenti |
|
Informazioni sullo studio clinico
(dati da https://clinicaltrials.gov, aggiornato il 2024-05-22)
| Numero NCT | Reclutamento | Condizioni | Sponsor/Collaboratori | Data di inizio | Fasi |
|---|---|---|---|---|---|
| NCT06193863 | Not yet recruiting | Prevention of Venous Thromboembolism|Congenital Heart Disease|Fontan Procedure|Children |
Bayer|Janssen Research & Development LLC |
May 31 2024 | -- |
| NCT06195540 | Not yet recruiting | Venous Thromboembolism|Deep Vein Thrombosis|Pulmonary Embolism|Lower Limb Trauma|Thromboprophylaxis|Immobilisation |
University Hospital Angers |
May 31 2024 | Phase 3 |
| NCT06314763 | Completed | Drug Drug Interaction Study |
Radboud University Medical Center|Amgen |
November 9 2023 | Phase 4 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
