solo per uso di ricerca
LY2811376 BACE inibitore
N. Cat.S1528
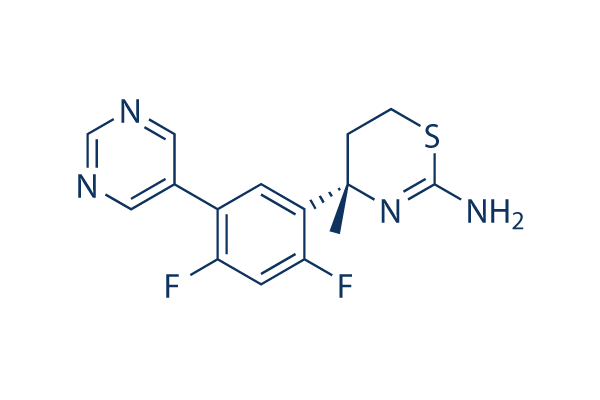
Struttura chimica
Peso molecolare: 320.36
Controllo Qualità
| Target correlati | HDAC Caspase Proteasome Secretase MMP HCV Protease Cysteine Protease DPP Tyrosinase HIV Protease |
|---|---|
| Altro BACE Inibitori | Verubecestat (MK-8931) LY2886721 Verubecestat (MK-8931) Trifluoroacetate AZD3839 Lanabecestat (AZD3293) Elenbecestat Loganin LX2343 |
Coltura cellulare, trattamento e concentrazione di lavoro
| Linee cellulari | Tipo di saggio | Concentrazione | Tempo di incubazione | Formulazione | Descrizione dellattività | PMID |
|---|---|---|---|---|---|---|
| HEK293 cells | Function assay | Inhibition of BACE1 in HEK293 cells expressing APPswedish mutant assessed as inhibition of amyloid beta production by ELISA, EC50=0.3 μM | ||||
| Clicca per visualizzare più dati sperimentali sulle linee cellulari | ||||||
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 320.36 | Formula | C15H14F2N4S |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 1194044-20-6 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
| Sinonimi | N/A | Smiles | CC1(CCSC(=N1)N)C2=C(C=C(C(=C2)C3=CN=CN=C3)F)F | ||
Solubilità
|
In vitro |
Ethanol : 64 mg/mL
DMSO
: 16 mg/mL
(49.94 mM)
Water : Insoluble |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Caratteristiche |
Approximately 10-fold selectivity toward BACE1 over BACE2.
|
|---|---|
| Targets/IC50/Ki |
BACE1
239 nM-249 nM
Aβ
~300 nM(EC50)
|
| In vitro |
LY2811376 dimostra un'inibizione dose-dipendente di hBACE1 con una IC50 di 239 e 249 nM rispettivamente contro un piccolo peptide sintetico o un substrato proteico chimerico più grande. Il trattamento con questo composto produce una diminuzione dose-dipendente della secrezione di Beta Amyloid nelle cellule HEK293 che sovraesprimono APP. Inibisce la secrezione di Beta Amyloid con una EC50 di circa 100 nM in colture neuronali primarie di topi transgenici PDAPP.
|
| Saggio chinasico |
Determinazione dell'efficienza enzimatica
|
|
La soluzione madre per ogni substrato peptidico FRET è preparata a 30 mM in dimetilsolfossido (DMSO). La preparazione huBACE1:Fc muBACE1:Fc viene concentrata tramite YM10 Centricon. a una concentrazione finale di almeno 7 mg/mL. La concentrazione ottimale di enzima per ogni substrato peptidico FRET viene determinata individualmente a 30 μM di substrato peptidico FRET in 50 mM di acetato di ammonio, pH 4,6, 1 mg/mL di BSA e 1 mM di Triton X-100. L'efficienza enzimatica (kcat /Km) di uno o l'altro degli ortologhi di BACE1 verso i singoli substrati peptidici FRET a 15, 30 e 100 μM viene determinata nelle condizioni ottimali per ogni substrato. Il progresso della reazione viene monitorato misurando un aumento del segnale di emissione a 420 nm con lunghezza d'onda di eccitazione impostata a 320 nm, utilizzando un lettore di piastre a fluorescenza GEMINI. L'aminobenzoato coniugato con aminoacidi viene utilizzato per convertire il segnale di emissione nelle unità di fluorescenza relativa nella concentrazione molare del prodotto generato nella miscela di reazione. La fase iniziale della curva di dipendenza dal tempo viene adattata con una funzione lineare la cui pendenza viene utilizzata per calcolare la velocità iniziale per huBACE1:Fc verso ogni substrato peptidico. I valori di kcat /Km vengono calcolati dalla dipendenza lineare della velocità iniziale dalla concentrazione di ogni peptide.
|
|
| In vivo |
La somministrazione di LY2811376 (dosi di 10, 30 e 100 mg/kg) produce riduzioni significative e dose-dipendenti di Beta Amyloid, nonché di sAPPβ e C99, i prodotti di scissione prossimali della proteolisi di APP da parte di BACE1 nel modello murino APPV717F di patologia da Beta Amyloid. Dopo il trattamento con questo composto (5 mg/kg), si osservano riduzioni di Beta Amyloid1-x nel plasma, con una riduzione massima dell'85% osservata da 4 a 12 ore dopo la somministrazione nei cani beagle.
|
Riferimenti |
|
Informazioni sullo studio clinico
(dati da https://clinicaltrials.gov, aggiornato il 2024-05-22)
| Numero NCT | Reclutamento | Condizioni | Sponsor/Collaboratori | Data di inizio | Fasi |
|---|---|---|---|---|---|
| NCT00838084 | Completed | Alzheimer''s Disease |
Eli Lilly and Company |
December 2008 | Phase 1 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
