solo per uso di ricerca
lurasidone Dopamine Receptor antagonista
N. Cat.S5714
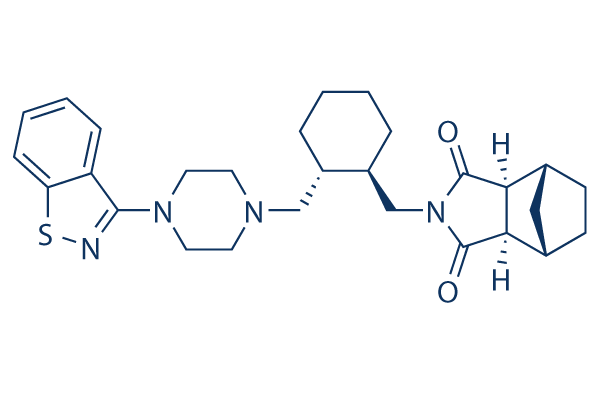
Struttura chimica
Peso molecolare: 492.68
Controllo Qualità
- Citato in Nature Medicine per la sua qualità superiore
- COA
- SDS
- Scheda tecnica
| Target correlati | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Histamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Altro Dopamine Receptor Inibitori | MPTP Hydrochloride Trifluoperazine Trifluoperazine 2HCl Penfluridol Sulpiride Levosulpiride SCH-23390 hydrochloride Domperidone Rotundine Azaperone |
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 492.68 | Formula | C28H36N4O2S |
Conservazione (Dalla data di ricezione) | 3 years -20°C powder |
|---|---|---|---|---|---|
| N. CAS | 367514-87-2 | -- | Conservazione delle soluzioni stock |
|
|
| Sinonimi | SM-13496 | Smiles | C1CCC(C(C1)CN2CCN(CC2)C3=NSC4=CC=CC=C43)CN5C(=O)C6C7CCC(C7)C6C5=O | ||
Solubilità
|
In vitro |
DMSO
: 7 mg/mL
(14.2 mM)
Water : Insoluble Ethanol : Insoluble |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Targets/IC50/Ki |
5-HT2A
(Cell-free assay) 0.5 nM(Ki)
5-HT7 receptor
(Cell-free assay) 0.5 nM(Ki)
D2 receptor
(Cell-free assay) 1 nM(Ki)
5-HT1A receptor
(Cell-free assay) 6.4 nM(Ki)
|
|---|---|
| In vitro |
Lurasidone è un nuovo antipsicotico atipico nella classe chimica dei benzoisotiazoli. Come la maggior parte degli antipsicotici di seconda generazione, è un antagonista completo dei recettori dopamina D2 e serotonina 5-HT2A, ed è un agonista parziale dei recettori 5-HT1A. Ha un'affinità molto maggiore per i recettori del sottotipo 5-HT7 rispetto ad altri antipsicotici atipici. Questo composto ha anche un'elevata affinità per il sottotipo 5-HT1A, i recettori "2c-adrenergici e una bassa affinità per i recettori "1-adrenergici. Ha un'affinità minima per i recettori 5-HT2C e un'affinità trascurabile per i recettori istaminici H1 e muscarinici.
|
| In vivo |
Lurasidone viene rapidamente assorbito, raggiungendo le concentrazioni di picco entro 1,5–3 ore (tmax) dopo dosi orali singole e multiple. Una volta assorbito, si distribuisce ampiamente nei tessuti ed entra rapidamente nel SNC. Questo composto ha un elevato legame con l'albumina plasmatica umana e l'alfa-1-glicoproteina (">=99%). Il trattamento a lungo termine della schizofrenia con questo agente ha dimostrato di ridurre il rischio di ricaduta. L'emivita di eliminazione di questa sostanza chimica è di circa 20-40 ore. La Cmax media e l'area sotto la curva (AUC) per questo farmaco sono state circa tre volte e due volte maggiori, rispettivamente, in un confronto tra somministrazione con cibo e a digiuno. Il suo assorbimento è indipendente dal contenuto di grassi del cibo. Viene metabolizzato principalmente tramite CYP3A4. Negli studi sugli animali, questo composto ha penetrato la barriera placentare e si è distribuito nel feto, ed è stato escreto nel latte durante l'allattamento.
|
Riferimenti |
|
Informazioni sullo studio clinico
(dati da https://clinicaltrials.gov, aggiornato il 2024-05-22)
| Numero NCT | Reclutamento | Condizioni | Sponsor/Collaboratori | Data di inizio | Fasi |
|---|---|---|---|---|---|
| NCT03627195 | Completed | Schizophrenia |
Sumitomo Pharma America Inc. |
June 7 2018 | Phase 1 |
| NCT02731612 | Recruiting | Bipolar Disorder |
Nazlin Walji|University of British Columbia |
May 8 2017 | Phase 3 |
| NCT02147379 | Completed | Bipolar I Disorder |
University of British Columbia |
May 2014 | Phase 3 |
| NCT02174523 | Completed | Schizophrenia |
Sumitomo Pharma (Suzhou) Co. Ltd.|Xuhui Central Hospital Shanghai |
April 2014 | Phase 1 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
