solo per uso di ricerca
Cinacalcet (AMG-073) HCl CaSR attivatore
N. Cat.S1260
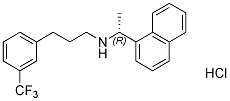
Struttura chimica
Peso molecolare: 393.87
Controllo Qualità
| Target correlati | CXCR Hedgehog/Smoothened PKA Adrenergic Receptor AChR 5-HT Receptor Histamine Receptor Dopamine Receptor Ras KRas |
|---|---|
| Altro CaSR Inibitori | NPS-2143 Evocalcet |
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 393.87 | Formula | C22H22F3N.HCl |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 364782-34-3 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
| Sinonimi | Mimpara, Sensipar,AMG-073 | Smiles | CC(C1=CC=CC2=CC=CC=C21)NCCCC3=CC(=CC=C3)C(F)(F)F.Cl | ||
Solubilità
|
In vitro |
DMSO
: 79 mg/mL
(200.57 mM)
Ethanol : 79 mg/mL Water : Insoluble |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Targets/IC50/Ki |
CaSR
2.8 μM(EC50)
|
|---|---|
| In vitro |
AMG-073 rappresenta una nuova classe di composti per il trattamento dell'iperparatiroidismo noti come calcimimetici, che riducono la sintesi e la secrezione dell'ormone paratiroideo (PTH) aumentando la sensibilità del recettore di rilevamento del calcio paratiroideo (CaSR) al calcio extracellulare. AMG-073 presenta potenziali vantaggi come terapia per l'iperparatiroidismo secondario perché mima gli effetti del calcio extracellulare per sopprimere la secrezione di PTH, anche in presenza di iperfosfatemia, senza il rischio di causare ipercalcemia e/o iperfosfatemia. AMG-073 produce un aumento calcio citoplasmatico dipendente dalla concentrazione nelle cellule renali embrionali umane che esprimono il CaSR. Nelle cellule paratiroidee bovine e in un tampone contenente calcio 0,5 mM, AMG-073 (3 nM – 1 μM) produce una diminuzione dei livelli di PTH dipendente dalla concentrazione con una IC50 di 27 nM. |
| In vivo |
AMG-073 somministrato oralmente a ratti normali a dosi di 1, 3, 10 e 30 mg/kg in 20% di sodio solfobutil etere β-ciclodestrina produce una significativa riduzione dose-dipendente dei livelli di PTH per 1-4 ore dopo la somministrazione. A 8 ore, le dosi di 10 e 30 mg/kg di AMG-073 producono riduzioni significative dei livelli di PTH rispetto ai controlli che scompaiono entro 24 ore. Si osservano riduzioni significative dose-dipendenti dei livelli di calcio sierico a 4, 8 e 24 ore dopo la somministrazione orale di AMG-073 3, 10 e 30 mg/kg, rispettivamente. Una riduzione transitoria dei livelli di fosforo sierico si osserva solo con la dose più alta di AMG-073. Inoltre, si osservano livelli aumentati di calcitonina che parallelamente sopprimono il PTH con AMG-073 40 mg/kg nei ratti. Come nei ratti normali, si osserva una rapida riduzione dose-dipendente dei livelli di PTH e calcio in 5 su 6 ratti nefrectomizzati dopo somministrazione orale di AMG-073. Inoltre, AMG-073 orale a 5 e 10 mg/kg per 4 settimane riduce significativamente il peso della paratiroide rispetto ai controlli. |
Riferimenti |
|
Informazioni sullo studio clinico
(dati da https://clinicaltrials.gov, aggiornato il 2024-05-22)
| Numero NCT | Reclutamento | Condizioni | Sponsor/Collaboratori | Data di inizio | Fasi |
|---|---|---|---|---|---|
| NCT05926570 | Completed | Drug Effect |
Tanta University |
August 5 2023 | Phase 4 |
| NCT03123406 | Completed | Hyperparathyroidism; Secondary Renal |
Kyowa Kirin China Pharmaceutical Co. Ltd.|Kyowa Kirin Co. Ltd. |
April 19 2017 | Phase 4 |
| NCT02341417 | Completed | Secondary Hyperparathyroidism Chronic Kidney Disease |
Amgen |
June 10 2015 | Phase 3 |
| NCT01748812 | Terminated | Osteomalacia |
National Institute of Dental and Craniofacial Research (NIDCR)|National Institutes of Health Clinical Center (CC) |
November 16 2012 | Phase 1 |
| NCT01439867 | Terminated | Chronic Kidney Disease|Hyperparathyroidism Secondary |
Amgen |
June 22 2012 | Phase 2 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
