solo per uso di ricerca
Telbivudine Reverse Transcriptase inibitore
N. Cat.S1651
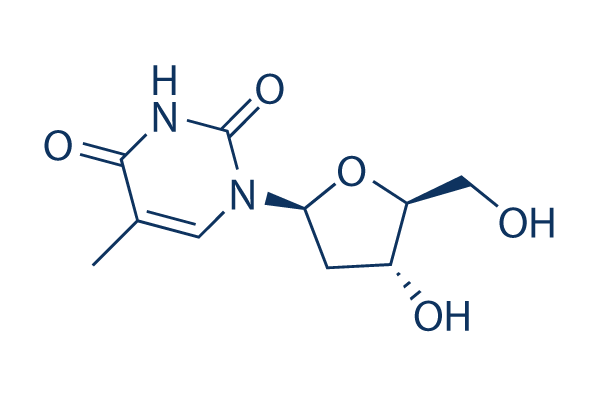
Struttura chimica
Peso molecolare: 242.23
Controllo Qualità
| Target correlati | Integrase Bacterial Antibiotics Anti-infection Fungal Antiviral COVID-19 Parasite HIV HCV Protease |
|---|---|
| Altro Reverse Transcriptase Inibitori | Dapivirine (TMC120) Fangchinoline Salicylanilide 3'-Fluoro-3'-deoxythymidine (Alovudine) Ulonivirine Lersivirine (UK-453061) Bifendate 4-Chloro-2-(trifluoroacetyl)aniline hydrochloride |
Informazioni chimiche, conservazione e stabilità
| Peso molecolare | 242.23 | Formula | C10H14N2O5 |
Conservazione (Dalla data di ricezione) | |
|---|---|---|---|---|---|
| N. CAS | 3424-98-4 | Scarica SDF | Conservazione delle soluzioni stock |
|
|
| Sinonimi | NV 02B | Smiles | CC1=CN(C(=O)NC1=O)C2CC(C(O2)CO)O | ||
Solubilità
|
In vitro |
DMSO
: 48 mg/mL
(198.15 mM)
Water : 48 mg/mL Ethanol : 2 mg/mL |
Calcolatore di Molarità
|
In vivo |
|||||
Calcolatore di formulazione in vivo (Soluzione chiara)
Passo 1: Inserire le informazioni di seguito (Consigliato: Un animale aggiuntivo per tenere conto della perdita durante lesperimento)
Passo 2: Inserire la formulazione in vivo (Questo è solo il calcolatore, non la formulazione. Contattateci prima se non cè una formulazione in vivo nella sezione Solubilità.)
Risultati del calcolo:
Concentrazione di lavoro: mg/ml;
Metodo per preparare il liquido master di DMSO: mg farmaco predissolto in μL DMSO ( Concentrazione del liquido master mg/mL, Vi preghiamo di contattarci prima se la concentrazione supera la solubilità del DMSO del lotto del farmaco. )
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungereμL PEG300, mescolare e chiarire, quindi aggiungereμL Tween 80, mescolare e chiarire, quindi aggiungere μL ddH2O, mescolare e chiarire.
Metodo per preparare la formulazione in vivo: Prendere μL DMSO liquido master, quindi aggiungere μL Olio di mais, mescolare e chiarire.
Nota: 1. Si prega di assicurarsi che il liquido sia limpido prima di aggiungere il solvente successivo.
2. Assicurarsi di aggiungere il/i solvente/i in ordine. È necessario assicurarsi che la soluzione ottenuta, nellaggiunta precedente, sia una soluzione limpida prima di procedere allaggiunta del solvente successivo. Metodi fisici come il vortex, gli ultrasuoni o il bagno dacqua calda possono essere utilizzati per facilitare la dissoluzione.
Meccanismo dazione
| Targets/IC50/Ki |
HBV RT
|
|---|---|
| In vitro |
Telbivudine mostra un'attività antivirale potente, selettiva e specifica contro l'HBV e altri virus hepadna. Questo composto viene fosforilato dalle timidina chinasi intracellulari nella forma trifosfato attiva, che ha un'emivita intracellulare di 14 ore. Il suo 5′-trifosfato inibisce la DNA polimerasi dell'HBV (reverse transcriptase) competendo con il substrato naturale, il dTTP. Questa sostanza chimica aumenta significativamente la produzione di fattore di necrosi tumorale-alfa e interleuchina-12 nei macrofagi indotti da MHV-3. Aumenta significativamente i livelli sierici di interferone-gamma. Questo trattamento migliora la capacità delle cellule T di proliferare e secernere citochine ma non influenza la citotossicità degli epatociti infetti. Sopprime l'espressione del ligando 1 della morte programmata sulle cellule T. Il composto rimane attivo come dimostrato dai rispettivi cambiamenti di 0,5 (N236T) e 1,0 (A181V e A194T). Non è attivo contro i ceppi di HBV che portano le mutazioni L180M/M204V/I della lamivudina ma rimane attivo contro il singolo mutante M204V in vitro, spiegando potenzialmente la differenza nei profili di resistenza tra Telbivudine e lamivudina. |
Riferimenti |
|
Informazioni sullo studio clinico
(dati da https://clinicaltrials.gov, aggiornato il 2024-05-22)
| Numero NCT | Reclutamento | Condizioni | Sponsor/Collaboratori | Data di inizio | Fasi |
|---|---|---|---|---|---|
| NCT02956850 | Completed | Hepatitis B Chronic |
Hoffmann-La Roche |
December 12 2016 | Phase 1 |
| NCT02894554 | Terminated | HBsAg-positive Renal Allograft Recipients |
National Taiwan University Hospital |
July 2014 | Phase 4 |
| NCT01379508 | Completed | Chronic Hepatitis B |
Novartis Pharmaceuticals|Novartis |
March 21 2011 | Phase 4 |
| NCT01163240 | Completed | Liver Diseases|Hepatitis Chronic|Hepatitis Viral Human|Hepatitis|Virus Diseases|Digestive System Diseases|Hepatitis B Chronic|Hepatitis B|DNA Virus Infections |
Novartis Pharmaceuticals|Novartis |
June 2009 | -- |
| NCT00877149 | Completed | Compensated Chronic Hepatitis B |
Novartis Pharmaceuticals|Novartis |
March 2009 | Phase 4 |
Supporto tecnico
Istruzioni per la manipolazione
Tel: +1-832-582-8158 Ext:3
Per qualsiasi altra domanda, si prega di lasciare un messaggio.
