uitsluitend voor onderzoeksdoeleinden
Simeprevir HCV Protease remmer
Cat.Nr.S5015
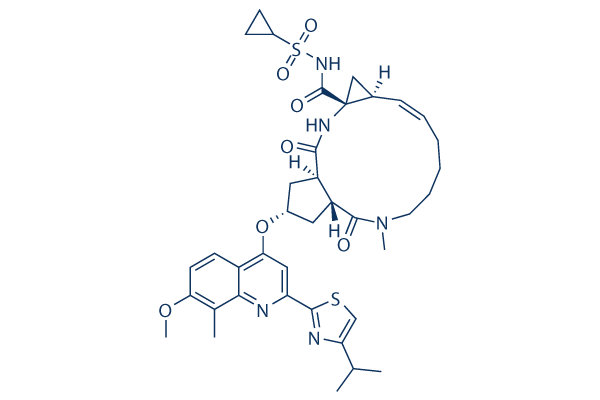
Chemische structuur
Moleculair gewicht: 749.94
Kwaliteitscontrole
| Gerelateerde doelwitten | HDAC Caspase Proteasome Secretase MMP Cysteine Protease DPP Tyrosinase HIV Protease Serine Protease |
|---|---|
| Overige HCV Protease Inhibitoren | Danoprevir Lomibuvir (VX-222) Asunaprevir Tizoxanide PSI-6206 (GS-331007) Mecarbinate Tegobuvir Herba taxilli Extract 2'-C-Methylcytidine |
Chemische informatie, Opslag en Stabiliteit
| Moleculair gewicht | 749.94 | Formule | C38H47N5O7S2 |
Opslag (Vanaf de ontvangstdatum) | |
|---|---|---|---|---|---|
| CAS-nr. | 923604-59-5 | -- | Opslag van stamoplossingen |
|
|
| Synoniemen | TMC435, TMC-435350 | Smiles | CC1=C(C=CC2=C1N=C(C=C2OC3CC4C(C3)C(=O)N(CCCCC=CC5CC5(NC4=O)C(=O)NS(=O)(=O)C6CC6)C)C7=NC(=CS7)C(C)C)OC | ||
Oplosbaarheid
|
In vitro |
DMSO
: 100 mg/mL
(133.34 mM)
Ethanol : 4 mg/mL Water : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo Formuleringscalculator (Heldere oplossing)
Stap 1: Voer de onderstaande informatie in (Aanbevolen: Een extra dier voor het geval van verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in het gedeelte Oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-mastervloeistof: mg geneesmiddel vooraf opgelost in μL DMSO ( Concentratie mastervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de partij geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toeμL PEG300, mengen en helder maken, voeg vervolgens toeμL Tween 80, mengen en helder maken, voeg vervolgens toe μL ddH2O, mengen en helder maken.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toe μL Maïsolie, mengen en helder maken.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysische methoden zoals vortexen, echografie of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
HCV NS3/4A protease
|
|---|---|
| In vitro |
Simeprevir vertoont een krachtige remming van NS3/4A Protease van genotypes 1a, 1b, 2, 4, 5 en 6, met een gemiddelde remmende concentratie (IC50) <13 nM voor alle geteste HCV NS3/4A-enzymen. Echter, de IC50 voor genotype 3 is 37 nM. In vitro is deze verbinding ook een remmer van bilirubine-transporters OATP1B1 en MRP2. Het is een krachtigere remmer van OATP1B1 (IC50=720 nM), dat voornamelijk verantwoordelijk is voor het transport van ongeconjugeerd bilirubine, dan MRP2 (IC50 rond 10.000 nM), voornamelijk een geconjugeerde bilirubine-transporter.
|
| In vivo |
In vivo heeft Simeprevir een relatief lange absorptiefase, waarbij de maximale concentratie (Cmax) na 4-6 uur wordt bereikt. Het is uitgebreid (99,9%) gebonden aan plasmaproteïnen, voornamelijk aan albumine. De absolute biologische beschikbaarheid is 44% na een eenmalige orale toediening. Bij ratten is de lever-bloedverhouding 29:1, wat een goede distributie naar de lever betekent. Voor mensen is in preklinische studies de lever-plasmaconcentratieverhouding erg hoog (verhouding van 39). De hoogste weefsel/plasma AUC-verhoudingen worden waargenomen in de dunne darm (verhouding van 128). Hoewel weefselconcentraties van deze verbinding piekwaarden bereiken binnen 4 uur na toediening, blijven de concentraties in de lever tot 31 uur na toediening boven de EC99, en plasmaconcentraties zijn hoger dan de EC99 na 8 uur en rond de EC50 na 24 uur na toediening. De AUC24h van deze chemische stof neemt met 61%-69% toe wanneer deze met voedsel wordt toegediend. Het moet daarom met voedsel worden ingenomen. Deze verbinding is ook een substraat en remmer van P-glycoproteïne. Het wordt gemetaboliseerd door CYP3A4 en geëlimineerd via biliaire excretie. Het is ook een remmer van het darmcytochroom 3A4, maar niet van hepatisch CYP3A4.
|
Referenties |
Informatie klinische proef
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Rekrutering | Aandoeningen | Sponsor/Medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT03277755 | Withdrawn | Hepatic Impairment |
Janssen Research & Development LLC |
September 11 2017 | Phase 1 |
| NCT02404805 | Completed | HIV|Hepatitis C |
University of Colorado Denver |
February 2016 | Not Applicable |
| NCT02569710 | Completed | Chronic Hepatitis C |
Alios Biopharma Inc. |
October 31 2015 | Phase 2 |
| NCT02512562 | Completed | Chronic Hepatitis C |
Alios Biopharma Inc.|Alexion Pharmaceuticals Inc. |
July 31 2015 | Phase 1 |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, kunt u een bericht achterlaten.
