réservé à la recherche
MK-2461 c-Met inhibiteur
N° Cat.S2774
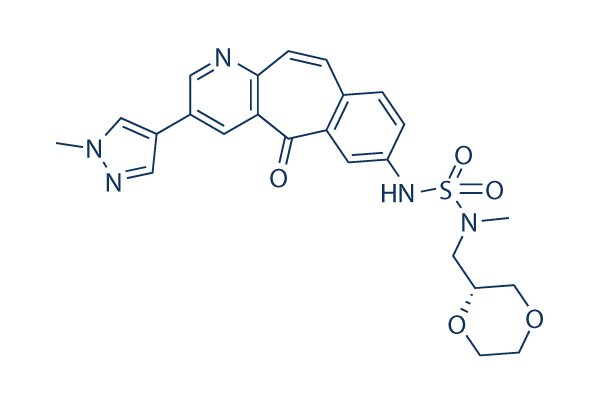
Structure chimique
Poids moléculaire: 495.55
Contrôle qualité
| Cibles apparentées | EGFR VEGFR PDGFR FGFR Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Autre c-Met Inhibiteurs | Tepotinib Dihexa SGX-523 PHA-665752 Foretinib SU11274 BMS-777607 JNJ-38877605 Tivantinib PF-04217903 |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 495.55 | Formule | C24H25N5O5S |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 917879-39-1 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | CN1C=C(C=N1)C2=CC3=C(C=CC4=C(C3=O)C=C(C=C4)NS(=O)(=O)N(C)CC5COCCO5)N=C2 | ||
Solubilité
|
In vitro |
DMSO
: 99 mg/mL
(199.77 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Fonctionnalités |
Preferentially binds to activated c-Met, distinguished from other known ATP-competitive tyrosine kinase inhibitors (which bind to inactive and active kinases with similar affinity).
|
|---|---|
| Targets/IC50/Ki |
c-Met (M1250T)
0.4 nM
c-Met (Y1235D)
0.5 nM
c-Met (Y1230H)
1.0 nM
c-Met (N1100)
1.5 nM
c-Met (Y1230C)
1.5 nM
c-Met
2.5 nM
RON
7 nM
FLT1
10 nM
FLT3
22 nM
PDGFRβ
22 nM
Mer
24 nM
FGFR2
39 nM
KDR
44 nM
TrkA
46 nM
FGFR3
50 nM
TrkB
61 nM
FGFR1
65 nM
FLT4
78 nM
DRAK1
199 nM
JAK2
225 nM
|
| In vitro |
Le MK-2461 inhibe également puissamment FGFR1, FGFR2, FGFR3, KDR, TrkA, TrkB et Flt4 avec une IC50 de 65 nM, 39 nM, 50 nM, 44 nM, 46 nM, 61 nM et 78 nM, respectivement. Comparé au c-Met de type sauvage, ce composé inhibe plus puissamment l'activité des mutants kinase c-Met oncogènes tels que N1100Y, Y1230C, Y1230H, Y1235D et M1250T avec une IC50 de 1,5 nM, 1,5 nM, 1,0 nM, 0,5 nM et 0,4 nM, respectivement. Il se lie plus fortement au c-Met phosphorylé qu'au c-Met non phosphorylé. Ce produit chimique inhibe puissamment l'autophosphorylation induite par l'ATP du domaine de liaison COOH-terminal du c-Met, mais pas la boucle d'activation. En revanche, il inhibe la phosphorylation de la boucle d'activation de FGFR2 (Y653/Y654) dans les cellules Kato III et de PDGFRα (Y849) dans les cellules H1703 avec une IC50 de <0,3 μM. Il inhibe la mitogenèse induite par le HGF des cellules 4MBr-5 avec une IC50 de 204 nM, et la migration induite par le HGF des cellules HPAF II avec une IC50 de 404 nM, ainsi que la tubulogenèse ramifiée induite par le HGF des cellules MDCK. De plus, ce composé inhibe puissamment la prolifération indépendante de l'IL-3 des cellules 32D transformées avec le mutant Tpr-Met ou Tpr-Met (Y362C) avec une IC50 de ~100 nM. Il inhibe significativement la prolifération d'un large panel de lignées de cellules tumorales, particulièrement puissant contre les cellules tumorales hébergeant une amplification génomique de MET ou FGFR2.
|
| Kinase Assay |
Test de transfert d'énergie par résonance de fluorescence résolue dans le temps
|
|
La phosphorylation catalysée par c-Met du peptide N-biotinylé (EQEDEPEGDYFEWLE-CONH2) est mesurée à l'aide d'un test de transfert d'énergie par résonance de fluorescence résolue dans le temps. Les IC50 de ce composé pour Ron, Mer, Flt1, Flt3, Flt4, KDR, PDGFRβ, FGFR1, FGFR2, FGFR3, TrkA et TrkB sont déterminées à l'aide de tests de transfert d'énergie par résonance de fluorescence résolue dans le temps similaires au test de la kinase c-Met.
|
|
| In vivo |
Le traitement au MK-2461 inhibe significativement la phosphorylation de c-Met (Y1349) dans les tumeurs GTL-16 avec une IC50 d'environ 1 μM. L'administration orale de ce composé à 10 mg/kg, 50 mg/kg et 100 mg/kg deux fois par jour, ainsi qu'à 200 mg/kg une fois par jour, supprime efficacement la croissance tumorale des xénogreffes GTL-16 chez la souris de 62 %, 77 %, 75 % et 90 %, respectivement. De même, ce traitement chimique à 134 mg/kg deux fois par jour inhibe la croissance des tumeurs NIH3T3 hébergeant les mutants à un seul nucléotide c-Met T3936C et T3997C, de 78 % et 62 %, respectivement.
|
Références |
|
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT00496353 | Completed | Neoplasm |
Merck Sharp & Dohme LLC |
June 2007 | Phase 1|Phase 2 |
| NCT00518739 | Completed | Advanced Cancer |
Merck Sharp & Dohme LLC |
February 2007 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
