uitsluitend voor onderzoeksdoeleinden
ASP2215 (Gilteritinib) FLT3/AXL-remmer
Cat.Nr.S7754
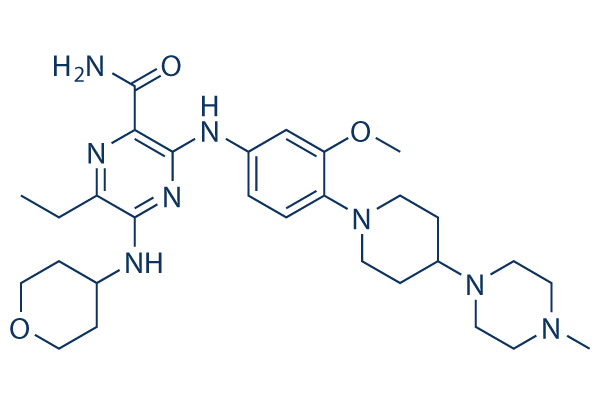
Chemische structuur
Moleculair gewicht: 552.71
Kwaliteitscontrole
Producten Vaak Samen Gebruikt Met ASP2215 (Gilteritinib)
| Gerelateerde doelwitten | EGFR VEGFR PDGFR FGFR c-Met Src MEK CSF-1R HER2 c-Kit |
|---|---|
| Overige FLT3 Inhibitoren | UNC2025 Crenolanib (CP-868596) Dovitinib (TKI-258) Dovitinib (TKI258) Lactate monohydrate Tandutinib (MLN518) KW-2449 ENMD-2076 AST-487 (NVP-AST487) TCS 359 G-749 |
Celkweek, behandeling & werkconcentratie
| Cellijnen | Assaytype | Concentratie | Incubatietijd | Formulering | Activiteitsbeschrijving | PMID |
|---|---|---|---|---|---|---|
| MV4-11 cells | Cell cycle assay | 1, 3, 10, and 30 nM | 24 h | The mean proportion of MV4-11 cells in G1 phase were significantly increased at gilteritinib concentrations of 3 (69.0%; P<0.01) and 10 nM (70.7%; P<0.001). | 31069015 | |
| MOLM-13 cells | Apoptosis assay | 1, 3, 10, 30, and 100 nM | 48 h | significant increases in the percentage of annexin V-positive cells at concentrations of 30 nM (32.0%) and 100 nM (52.4%) versus control (4.1%) | 31069015 | |
| 32D/TKD cells | Function assay | 50 nM | 6 h | Inhibiton of the phosphorylation of Akt on T308 | 29507660 | |
| TF-1 cells | Function assay | 0, 20, 80, 200 and 500 nM | 1 h | gilteritinib has an IC50 against wild-type c-Kit of 102 nM | 27908881 | |
| BA/F3 | Function assay | Inhibition Assay: A recombinant retrovirus was created from expression plasmid FLAG-EML4-ALKv1/pMX-iresCD8 in which cDNA for EMLA-ALK fusion protein v1 was integrated, and injected into mouse lymphoid cell line BA/F3 cells. Using a magnetic bead reagent f, IC50 = 0.0015 μM. | ChEMBL | |||
| BA/F3 | Function assay | Inhibition Assay: A recombinant retrovirus was created from expression plasmid FLAG-EML4-ALKv1/pMX-iresCD8 in which cDNA for EMLA-ALK fusion protein v1 was integrated, and injected into mouse lymphoid cell line BA/F3 cells. Using a magnetic bead reagent f, IC50 = 0.0015 μM. | ChEMBL | |||
| Vero | Antiviral assay | 24 hr | Antiviral activity against SARS-CoV-2 (viral titer) measured by plaque assay in Vero cells at MOI 0.0125 after 24 hr, IC50 = 6.76 μM. | ChEMBL | ||
| Vero | Cell viability assay | 72 hr | Cell viability measured by CellTiter-Glo assay in Vero cells at MOI 0.05 after 72hr, CC50 = 37.16 μM. | ChEMBL | ||
| Klik om meer experimentele gegevens over de cellijn te bekijken | ||||||
Chemische informatie, Opslag en Stabiliteit
| Moleculair gewicht | 552.71 | Formule | C29H44N8O3 |
Opslag (Vanaf de ontvangstdatum) | |
|---|---|---|---|---|---|
| CAS-nr. | 1254053-43-4 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | N/A | Smiles | CCC1=C(N=C(C(=N1)C(=O)N)NC2=CC(=C(C=C2)N3CCC(CC3)N4CCN(CC4)C)OC)NC5CCOCC5 | ||
Oplosbaarheid
|
In vitro |
DMSO
: 4 mg/mL
(7.23 mM)
Water : Insoluble Ethanol : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo Formuleringscalculator (Heldere oplossing)
Stap 1: Voer de onderstaande informatie in (Aanbevolen: Een extra dier voor het geval van verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in het gedeelte Oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-mastervloeistof: mg geneesmiddel vooraf opgelost in μL DMSO ( Concentratie mastervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de partij geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toeμL PEG300, mengen en helder maken, voeg vervolgens toeμL Tween 80, mengen en helder maken, voeg vervolgens toe μL ddH2O, mengen en helder maken.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toe μL Maïsolie, mengen en helder maken.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysische methoden zoals vortexen, echografie of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
FLT3
(Cell-free assay) 0.29 nM
Axl
(Cell-free assay) 0.73 nM
|
|---|---|
| In vitro |
Gilteritinib (ASP2215) vertoont een potente remmende activiteit tegen de interne tandem duplicatie (FLT3-ITD) en FLT3-D835Y puntmutaties in cel assays met MV4-11 en MOLM-13 cellen, evenals Ba/F3 cellen die gemuteerd FLT3 tot expressie brengen. Het verlaagt de fosforyleringsniveaus van FLT3 en zijn downstream targets in zowel cellulaire als diermodellen. Deze verbinding remt de activiteit van acht van de 78 geteste kinasen met meer dan 50% bij concentraties van ofwel 1 nM (FLT3, LTK, ALK, en AXL) of 5 nM (TRKA, ROS, RET, en MER). Behandeling ermee gedurende 48 uur resulteert in een inductie van apoptose in MV4-11 cellen, zoals bepaald door een toename van annexine V-positieve cellen. Het vermindert ook de expressie van anti-apoptotische eiwitten zoals MCL-1, BCL2L10, en survivin, die naar verluidt belangrijk zijn voor chemotherapiegevoeligheid, na 24 uur behandeling.
|
| In vivo |
In vivo wordt gilteritinib (ASP2215) na orale toediening in hoge mate verdeeld in xenografted tumoren. De verminderde FLT3-activiteit en hoge intratumorale distributie van deze verbinding vertaalt zich in tumorregressie en verbeterde overleving in xenograft- en intra-botmergtransplantatiemodellen van FLT3-gedreven AML. Deze antitumoractiviteit is geassocieerd met een duurzame remming van phospho-FLT3 en phospho-STAT5. Bovendien vermindert behandeling ermee de leukemische belasting en verlengt het de overleving in een muis IBMT-model. Geen duidelijke toxiciteit wordt waargenomen in muismodellen behandeld met gilteritinib.
|
Referenties |
|
Toepassingen
| Methoden | Biomarkers | Afbeeldingen | PMID |
|---|---|---|---|
| Western blot | p-STAT5 / STAT5 / p-AKT / AKT / p-ERK / ERK p-c-kit / c-kit p-FLT3(Y591) / FLT3 |
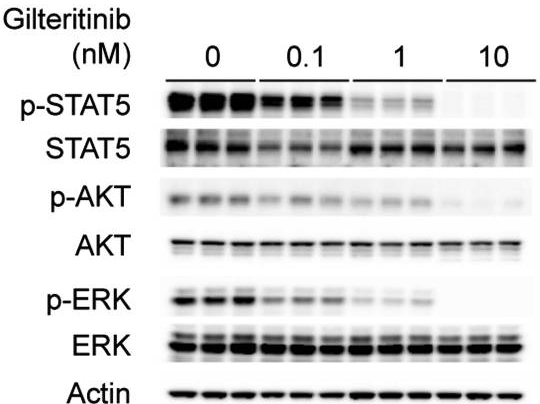
|
28516360 |
Informatie klinische proef
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Rekrutering | Aandoeningen | Sponsor/Medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT06022003 | Recruiting | AML Adult|Refractory AML|Relapsed Adult AML|FLT3-TKD Mutation|FLT3-ITD |
French Innovative Leukemia Organisation|Acute Leukemia French Association |
January 13 2024 | Phase 2 |
| NCT05520567 | Recruiting | Acute Myeloid Leukemia (AML)|FLT3-mutated Acute Myeloid Leukemia |
Astellas Pharma Global Development Inc.|Astellas Pharma Inc |
January 27 2023 | Phase 1|Phase 2 |
| NCT05791890 | Active not recruiting | Acute Myeloid Leukemia |
University of Rome Tor Vergata |
May 31 2022 | -- |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, kunt u een bericht achterlaten.
