réservé à la recherche
Apigenin P450 (e.g. CYP17) inhibiteur
N° Cat.S2262
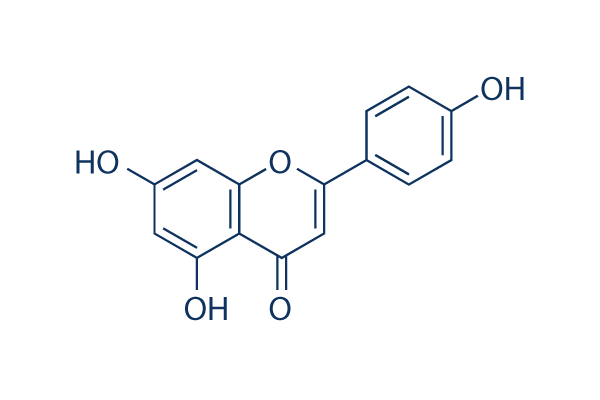
Structure chimique
Poids moléculaire: 270.24
Contrôle qualité
| Cibles apparentées | Dehydrogenase HSP Transferase PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism Drug Metabolite |
|---|---|
| Autre P450 (e.g. CYP17) Inhibiteurs | Baicalein Avasimibe Naringenin Diosmetin Alizarin Orteronel Benzbromarone Sodium Danshensu Naringin Piperine |
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| mouse RAW264.7 cells | Function assay | Inhibition of COX2 protein expression in mouse RAW264.7 cells, IC50=0.5 μM | ||||
| human H295R cells | Function assay | Inhibition of aromatase expressed in human H295R cells, IC50=1 μM | ||||
| HEK293 FS cells | Function assay | Inhibition of NOX4 expressed in HEK293 FS cells assessed as H2O2 production by H2O2/Tyr/LPO assay, IC50=1.13 μM | ||||
| human HeLa cells | Function assay | Inhibition of MRP1 transfected in human HeLa cells assessed as inhibition of [3H]LTC4 transport by rapid filtration assay, Ki=2.4 μM | ||||
| human MV4-11 cells | Cytotoxicity assay | 72 h | Cytotoxicity against human MV4-11 cells harboring FLT3 mutation after 72 hrs by tetrazolium based Ez CyTox cell viability assay, GI50=2.81 μM | |||
| human mast cells | Function assay | Inhibition of SYK in human mast cells assessed as reduction in mast cell degranulation, EC50=3 μM | ||||
| MDCK cells | Function assay | Inhibition of BCRP expressed in MDCK cells using Hoechst 33342 staining, IC50=3.1 μM | ||||
| human MDA-kb2 cells | Function assay | Antagonist activity at androgen receptor in human MDA-kb2 cells assessed as inhibition of DHT-induced luciferase activity by luciferase reporter gene assay, IC50=5.2 μM | ||||
| MCF-7 MX cells | Function assay | Inhibition of BCRP expressed in MCF-7 MX cells using Hoechst 33342 staining, IC50=5.9 μM | ||||
| mouse RAW264.7 cells | Function assay | 24 h | Antiinflammatory activity against mouse RAW264.7 cells assessed as inhibition of LPS-induced nitrite accumulation after 24 hrs by Griess reagent method, IC50=6.7 μM | |||
| human H9 cells | Function assay | 3 days | Antiviral activity against HIV1 3B infected in human H9 cells assessed as inhibition of viral replication after 3 days by p24 antigen capture assay, EC50=9 μM | |||
| HEK293 cells | Function assay | 24 h | Agonist activity at mouse PPARgamma expressed in HEK293 cells co-expressing with Gal4 reporter vector after 24 hrs by dual-luciferase reporter assay, EC50=24.9 μM | |||
| mouse 26-L5 cells | Proliferation assay | 72 h | Antiproliferative activity against mouse 26-L5 cells after 72 hrs by MTT assay, EC50=25 μM | |||
| human RS4:11 cells | Cytotoxicity assay | 72 h | Cytotoxicity against human RS4:11 cells harboring wild type FLT3 after 72 hrs by tetrazolium based Ez CyTox cell viability assay, GI50=27.9 μM | |||
| mouse B16-BL6 cells | Proliferation assay | 72 h | Antiproliferative activity against mouse B16-BL6 cells after 72 hrs by MTT assay, EC50=31.6 μM | |||
| human H9 cells | Cytotoxicity assay | 3 days | Cytotoxicity against human H9 cells after 3 days, IC50=35 μM | |||
| human HT1080 cells | Proliferation assay | 72 h | Antiproliferative activity against human HT1080 cells after 72 hrs by MTT assay, IC | |||
| MDCK cells | Cytotoxicity assay | Cytotoxicity against MDCK cells by MTT assay, CC50=39.59 μM | ||||
| mouse L929 cells | Function assay | 15 mins | Potentiation of recombinant human TNF-alpha-induced cytotoxicity of mouse L929 cells assessed as survivality preincubated for 15 mins before TNFalpha addition measured after 24 hrs by crystal violet staining | |||
| human THP1 cells | Function assay | 20 uM | 1 h | Inhibition of NOX2 in human THP1 cells assessed as downregulation of TPA-induced CD36 mRNA expression at 20 uM incubated for 1 hr prior to TPA challenge measured after 24 hrs by RT-PCR analysis | ||
| MDA-MB-231 cells | Function assay | 5 uM | Inhibition of PMA-stimulated NF-kappaB signaling (unknown origin) expressed in MDA-MB-231 cells at 5 uM incubated for 16 hrs by luciferase reporter gene assay | |||
| Cliquez pour voir plus de données expérimentales sur les lignées cellulaires | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 270.24 | Formule | C15H10O5 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 520-36-5 | Télécharger le SDF | Stockage des solutions mères |
|
|
Solubilité
|
In vitro |
DMSO
: 54 mg/mL
(199.82 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Fonctionnalités |
Much more potent than kaempferol and myricetin in CT-L inhibition.
|
|---|---|
| Targets/IC50/Ki |
CYP2C9
2 μM(Ki)
|
| In vitro |
Apigenin inhibe la PKC en compétition avec l'adénosine triphosphate (ATP). Ce composé réduit également le niveau de phosphorylation des protéines cellulaires stimulée par le TPA et inhibe l'expression de c-jun et c-fos induite par le TPA. Il exerce un effet de réversion sur la morphologie transformée des cellules NIH3T3 transformées par v-H-ras. Il a été démontré qu'il possède des propriétés antimutagènes dans un contexte de génotoxicité induite par le nitropyrène dans des cellules ovariennes de hamster chinois. Ce produit chimique supprime l'activité et l'expression de la cyclooxygénase-2 et de la monoxyde d'azote synthase-2 induites par le LPS dans les macrophages de souris. Il a été rapporté qu'il inhibe l'activité de la protéine kinase C, la protéine kinase activée par les mitogènes (MAPK), la transformation des fibroblastes embryonnaires de souris C3HI et les oncogènes en aval dans les cellules NIH3T3 transformées par v-Ha-ras. Ce composé bloque la kinase régulée par la prolifération des peroxysomes (ERK), une MAPK dans les hépatocytes isolés. Il a également été démontré qu'il régule à la baisse l'expression de l'échangeur Na+/Ca2+, une protéine importante pour l'extrusion du calcium dans les myocytes cardiaques de rats nouveau-nés. Il induit un arrêt réversible G2/M et G0/G1 en inhibant l'activité de la kinase p34 (cdc2), accompagné d'une stabilité accrue de la protéine p53 dans les cellules épidermiques et les fibroblastes. Il est également efficace pour inhiber la régulation positive de l'ICAM-1 induite par le TNFα dans les cellules endothéliales humaines cultivées. Il inhibe l'expression de HIF-1α et de VEGF via les voies PI3K/Akt/p70S6K1 et HDM2/p53 dans les cellules cancéreuses ovariennes humaines. Il inhibe la différenciation en supprimant la transduction du signal MAPK et en réduisant le niveau du facteur de transcription API dans les kératinocytes humains. Ce composé inhibe également la prolifération des kératinocytes humains.
|
| In vivo |
Apigenin régule à la baisse la production d'IL-4 chez les souris BALB/C immunisées à l'ovalbumine. Ce composé inhibe les métastases pulmonaires du mélanome en altérant l'interaction des cellules tumorales avec l'endothélium. Il a été démontré qu'il provoque une augmentation significative du poids utérin et de la concentration utérine globale du récepteur d'œstrogènes (ER)-α chez les souris femelles (64) et supprime également la croissance des cellules du cancer de la prostate et du sein par l'intermédiaire du récepteur d'œstrogènes β1. Ce produit chimique supprime les niveaux d'IGF-I dans les xénogreffes de tumeurs prostatiques et augmente les niveaux d'IGFBP-3, une protéine de liaison qui séquestre l'IGF-I dans la circulation vasculaire. Ce composé (12,5 mg/kg) augmente la prolifération cellulaire dans le gyrus denté de l'hippocampe de souris adultes.
|
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | MHC / MHC2A / MHC2B / MyoD CXCR4 CDK1 / Cyclin B1 / p21 |

|
29108230 |
| Immunofluorescence | E-caherin / Vimentin Snail |
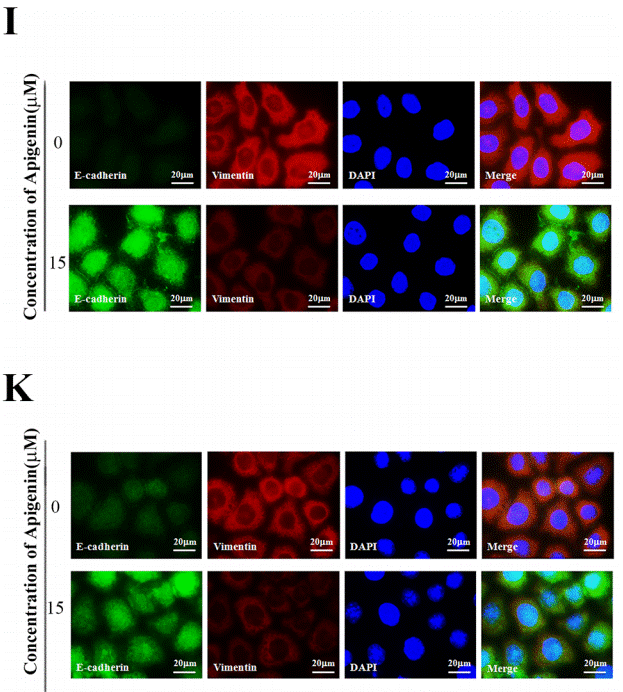
|
27203387 |
| Growth inhibition assay | Cell viability |
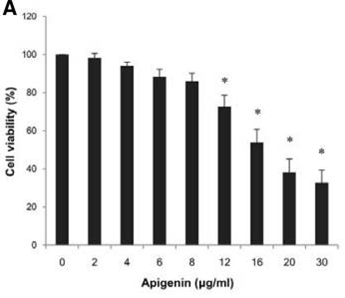
|
23224239 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
