Dati tecnici
| Formula | C19H21F2N7O2 |
||||||
| Peso molecolare | 417.41 | Numero CAS | 475110-96-4 | ||||
| Solubilità (25°C)* | In vitro | DMSO | 21 mg/mL (50.31 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Aggiungere i solventi al prodotto singolarmente e in ordine.) |
|
||||||
|
* <1 mg/ml significa leggermente solubile o insolubile. * Si prega di notare che Selleck testa la solubilità di tutti i composti internamente e la solubilità effettiva può differire leggermente dai valori pubblicati. Ciò è normale ed è dovuto a leggere variazioni da lotto a lotto. * Spedizione a temperatura ambiente (I test di stabilità mostrano che questo prodotto può essere spedito senza alcuna misura di raffreddamento.) |
|||||||
Preparazione delle soluzioni stock
Attività biologica
| Descrizione | ZSTK474 inibisce le isoforme di classe I della PI3K con una IC50 di 37 nM in un saggio senza cellule, principalmente PI3Kδ. Fase 1/2. | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Target |
|
||||||||||
| In vitro | ZSTK474 a 1 μM riduce potentemente l'attività di PI3K al 4,7% del livello di controllo, mentre LY2194002 riduce l'attività solo al 44,6% del controllo. Questo composto inibisce le attività delle p110β, -γ e -δ ricombinanti con IC50 di 17 nM, 53 nM e 6 nM, rispettivamente. Mostra una potente attività antiproliferativa contro un pannello di 39 linee cellulari di cancro umano con una GI50 media di 0,32 μM, più efficacemente rispetto a LY294002 o wortmannin con una GI50 media di 7,4 μM o 10 μM, rispettivamente. Questo trattamento chimico a 1 μM blocca il ruffling della membrana e la generazione di PIP3 indotta dal fattore di crescita derivato dalle piastrine in fibroblasti embrionali murini (MEF). A 10 μM induce l'apoptosi nelle cellule OVCAR3 e induce un arresto completo della fase G1 ma non l'apoptosi nelle cellule A549. Questo trattamento con il composto a 0,5 μM diminuisce significativamente il livello di Akt e GSK-3β fosforilati, così come l'espressione della proteina ciclina D1. Inibisce anche la fosforilazione di altri componenti di segnalazione a valle coinvolti nella regolazione della proliferazione cellulare, inclusi FKHRL1, FKHR, TSC-2, mTOR e p70S6K in modo dose-dipendente. Questa sostanza chimica non inibisce mTOR a 0,1 μM, e anche a una concentrazione di 100 μM, inibisce l'attività di mTOR meno del 40%. Blocca la migrazione cellulare indotta da VEGF e la formazione di tubi nelle cellule endoteliali della vena ombelicale umana (HUVEC), e inibisce l'espressione di HIF-1α e la secrezione di VEGF nelle cellule RXF-631L, esibendo una potente attività antiangiogenica in vitro. Questo trattamento con il composto inibisce la produzione di IFNγ e IL-17 nelle cellule T attivate dalla concanavalina A e inibisce la proliferazione e la produzione di PGE(2) da parte delle cellule sinoviali simili a fibroblasti (FLS). |
||||||||||
| In vivo | La somministrazione orale di ZSTK474 inibisce la crescita dei tumori di melanoma B16F10 di topo impiantati sottocute in modo dose-dipendente, producendo una regressione tumorale del 28,5%, 7,1% o 4,9% al giorno 14 a 100, 200 o 400 mg/kg, rispettivamente, il che è superiore a quello dei quattro principali farmaci antitumorali alle loro rispettive dosi massime tollerabili con una regressione tumorale del 96%, 35,7%, 24% o 68,3%, rispettivamente. Questo trattamento con il composto a 400 mg/kg inibisce completamente la crescita di xenotrapianti A549, PC-3 e WiDr nei topi e induce la regressione dei tumori xenotrapiantati A549. Inibisce significativamente la crescita tumorale nel modello di xenotrapianto RXF-631L, correlato a un numero significativamente ridotto di microvasi nei topi trattati. La somministrazione orale di questa sostanza chimica migliora la progressione dell'artrite indotta da adiuvante (AIA) nei ratti. | ||||||||||
| Caratteristiche | Primo inibitore di PI3K somministrato per via orale utilizzato in vivo. |
Protocollo (da riferimento)
| Saggio della chinasi: |
|
|---|---|
| Saggio cellulare: |
|
| Studio sugli animali: |
|
Riferimenti
|
Convalida del prodotto da parte del cliente
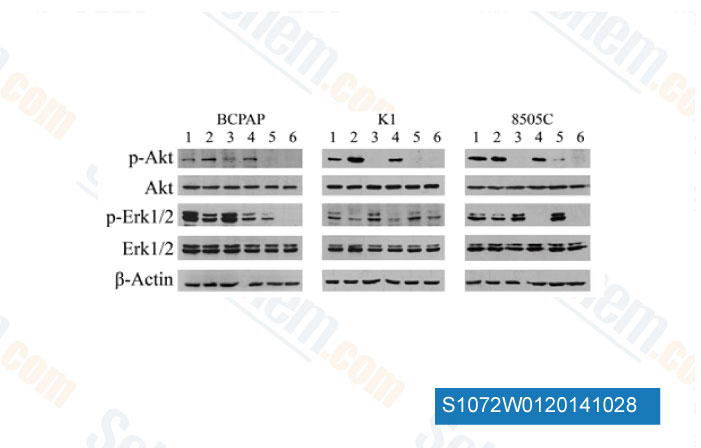
-
Dati da [ Invest New Drugs , 2014 , 32(4), 626-35 ]
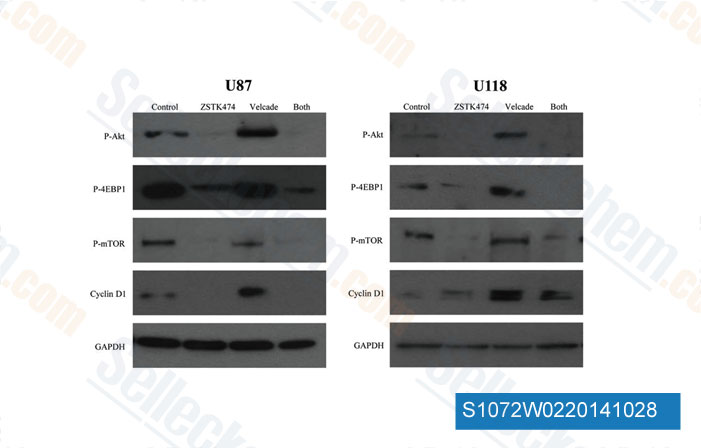
-
Dati da [ Int J Oncol , 2014 , 44(2), 557-62 ]
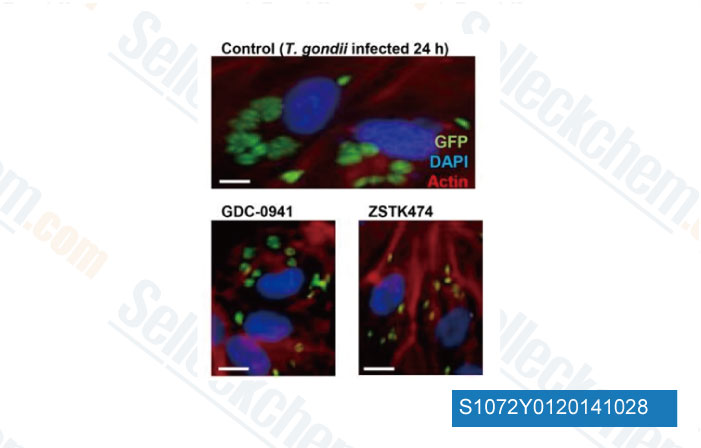
-
Dati da [ PLoS One , 2013 , 8(6), e66306 ]
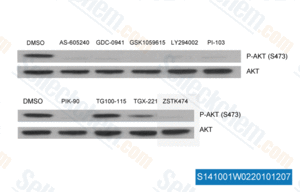
-
, , Saraswati Sukumar of Johns Hopkins University School of Medicine
Sellecks ZSTK474 È stato citato da 85 Pubblicazioni
| PI3K-Akt signalling regulates Scx-lineage tenocytes and Tppp3-lineage paratenon sheath cells in neonatal tendon regeneration [ Nat Commun, 2025, 16(1):3734] | PubMed: 40254618 |
| Perinatal thymic-derived CD8αβ-expressing γδ T cells are innate IFN-γ producers that expand in IL-7R-STAT5B-driven neoplasms [ Nat Immunol, 2024, 10.1038/s41590-024-01855-4] | PubMed: 38802512 |
| Perinatal thymic-derived CD8αβ-expressing γδ T cells are innate IFN-γ producers that expand in IL-7R-STAT5B-driven neoplasms [ Nat Immunol, 2024, 25(7):1207-1217] | PubMed: 38802512 |
| Reporter cell lines to screen for inhibitors or regulators of the KRAS-RAF-MEK1/2-ERK1/2 pathway [ Biochem J, 2024, 481(6):405-422] | PubMed: 38381045 |
| B cell adapter for PI 3-kinase (BCAP) coordinates antigen internalization and trafficking through the B cell receptor [ Sci Adv, 2024, 10(46):eadp1747] | PubMed: 39546610 |
| Multiplex single-cell chemical genomics reveals the kinase dependence of the response to targeted therapy [ Cell Genom, 2024, 4(2):100487] | PubMed: 38278156 |
| Stellettin B Sensitizes Glioblastoma to DNA-Damaging Treatments by Suppressing PI3K-Mediated Homologous Recombination Repair [ Adv Sci (Weinh), 2023, 10(3):e2205529] | PubMed: 36453577 |
| Young and undamaged recombinant albumin alleviates T2DM by improving hepatic glycolysis through EGFR and protecting islet β cells in mice [ J Transl Med, 2023, 21(1):89] | PubMed: 36747238 |
| HDAC Inhibition Restores Response to HER2-Targeted Therapy in Breast Cancer via PHLDA1 Induction [ Int J Mol Sci, 2023, 24(7)6228] | PubMed: 37047202 |
| Multiplex single-cell chemical genomics reveals the kinase dependence of the response to targeted therapy [ bioRxiv, 2023, 10.1101/2023.03.10.531983] | PubMed: None |
POLITICA DI RESO
La politica di reso incondizionato di Selleck Chemical garantisce ai nostri clienti unesperienza di acquisto online senza problemi. Se non sei in alcun modo soddisfatto del tuo acquisto, puoi restituire qualsiasi articolo entro 7 giorni dalla ricezione. In caso di problemi di qualità del prodotto, sia relativi al protocollo che al prodotto, puoi restituire qualsiasi articolo entro 365 giorni dalla data di acquisto originale. Si prega di seguire le istruzioni seguenti per la restituzione dei prodotti.
SPEDIZIONE E CONSERVAZIONE
I prodotti Selleck vengono trasportati a temperatura ambiente. Se ricevi il prodotto a temperatura ambiente, ti assicuriamo che il Dipartimento di Ispezione Qualità di Selleck ha condotto esperimenti per verificare che la conservazione a temperatura normale per un mese non influirà sullattività biologica dei prodotti in polvere. Dopo la raccolta, conservare il prodotto secondo le indicazioni descritte nella scheda tecnica. La maggior parte dei prodotti Selleck è stabile nelle condizioni raccomandate.
NON PER USO UMANO, DIAGNOSTICO VETERINARIO O TERAPEUTICO.
