Dati tecnici
| Formula | C18H18N2O3 |
||||||
| Peso molecolare | 310.35 | Numero CAS | 252916-29-3 | ||||
| Solubilità (25°C)* | In vitro | DMSO | 62 mg/mL (199.77 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Aggiungere i solventi al prodotto singolarmente e in ordine.) |
|
||||||
|
* <1 mg/ml significa leggermente solubile o insolubile. * Si prega di notare che Selleck testa la solubilità di tutti i composti internamente e la solubilità effettiva può differire leggermente dai valori pubblicati. Ciò è normale ed è dovuto a leggere variazioni da lotto a lotto. * Spedizione a temperatura ambiente (I test di stabilità mostrano che questo prodotto può essere spedito senza alcuna misura di raffreddamento.) |
|||||||
Preparazione delle soluzioni stock
Attività biologica
| Descrizione | Orantinib (SU6668) ha la maggiore potenza contro l'autofosforilazione di PDGFR con un Ki di 8 nM in un saggio acellulare, ma inibisce anche fortemente la trans-fosforilazione di Flk-1 e FGFR1. Mostra poca attività contro IGF-1R, Met, Src, Lck, Zap70, Abl e CDK2, e non inibisce EGFR. Questo composto è in Fase 3. | ||
|---|---|---|---|
| Target |
|
||
| In vitro | Orantinib (SU6668) è un inibitore competitivo, rispetto all'ATP, della trans-fosforilazione di Flk-1/KDR, della trans-fosforilazione di FGFR1 e dell'autofosforilazione delle chinasi PDGFRβ. Esso (0,03-10 μM) inibisce la fosforilazione della tirosina di KDR nelle HUVEC stimolate da VEGF. Questo composto inibisce anche la fosforilazione della tirosina di PDGFRβ stimolata da PDGF in cellule NIH-3T3 che sovraesprimono PDGFRβ a una concentrazione minima di 0,03-0,1 μM. Inibisce la fosforilazione indotta da FGF acido del substrato 2 di FGFR1 a 10 μM e superiori. Tuttavia, TSU-68 (fino a 100 μM) non ha alcun effetto sulla fosforilazione della tirosina di EGFR stimolata da EGF in cellule NIH-3T3 che sovraesprimono EGFR. Inibisce la mitogenesi delle HUVEC guidata da VEGF e FGF con IC50 medie rispettivamente di 0,34 μM e 9,6 μM. Nelle cellule MO7E di leucemia mieloide umana, questo composto inibisce l'autofosforilazione della tirosina del recettore del fattore delle cellule staminali (SCF), c-kit, con IC50 di 0,1-1 μM, così come la fosforilazione di ERK1/2, un evento di segnalazione a valle dell'attivazione di c-kit. Inibisce anche la proliferazione delle cellule MO7E indotta da SCF con IC50 di 0,29 μM, e induce apoptosi. | ||
| In vivo | Orantinib (SU6668) induce l'inibizione della crescita tumorale contro un'ampia gamma di tipi di tumore in modelli di xenotrapianto in topi atimici, incluse le cellule A375, Colo205, H460, Calu-6, C6, SF763T e SKOV3TP5 a dosi di 75-200 mg/kg. Questo composto (75 mg/kg) sopprime anche l'angiogenesi tumorale di xenotrapianti di glioma C6. In un modello tumorale di carcinoma del colon umano HT29, (200 mg/kg) diminuisce la permeabilità media dei vasi e il volume plasmatico frazionario medio nel bordo e nel nucleo del tumore. TSU-68 promuove lo sviluppo stromale anomalo alla periferia dei carcinomi. In un modello di tumore epatico VX2 di coniglio, (200 mg/kg) aumenta l'effetto dell'infusione chemioterapica. |
Protocollo (da riferimento)
| Saggio della chinasi: |
|
|---|---|
| Saggio cellulare: |
|
| Studio sugli animali: |
|
Riferimenti
|
Convalida del prodotto da parte del cliente
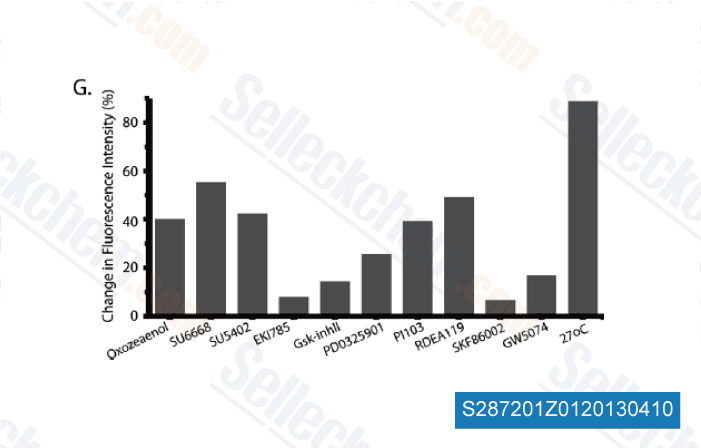
-
Dati da [ Mol Cell Proteomics , 2012 ]

-
Dati da [ Mol Cell Proteomics , 2012 ]
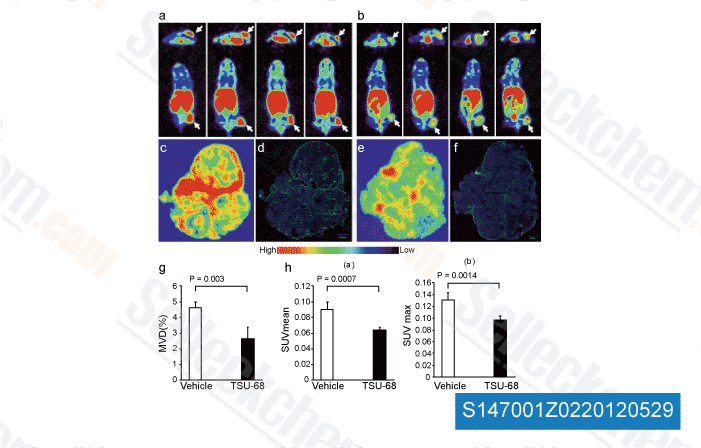
-
Dati da [ Angiogenesis , 2012 , 15, 569-80 ]
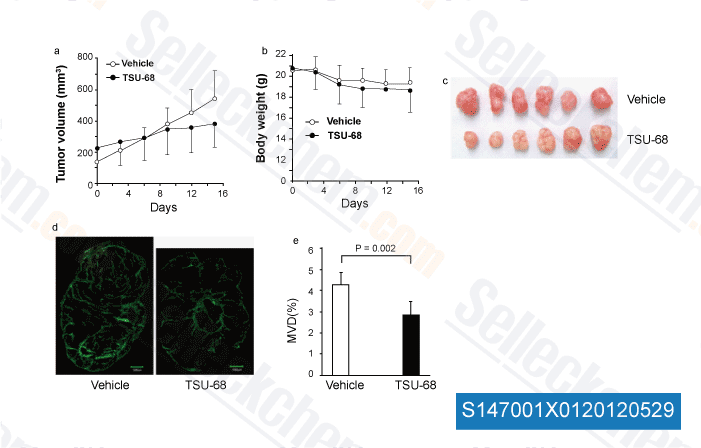
-
Dati da [ Angiogenesis , 2012 , 15, 569-80 ]
Sellecks Orantinib (SU6668) È stato citato da 21 Pubblicazioni
| SMYD5 is a novel epigenetic gatekeeper of the mild hypothermia response [ bioRxiv, 2023, 2023.05.11.540170] | PubMed: 37333301 |
| Establishment and Characterization of NCC-PMP1-C1: A Novel Patient-Derived Cell Line of Metastatic Pseudomyxoma Peritonei [ J Pers Med, 2022, 12(2)258] | PubMed: 35207746 |
| Establishment and characterization of NCC-UPS4-C1: a novel cell line of undifferentiated pleomorphic sarcoma from a patient with Li-Fraumeni syndrome [ Hum Cell, 2022, 10.1007/s13577-022-00671-y] | PubMed: 35118583 |
| Establishment and characterization of NCC-MFS4-C1: a novel patient-derived cell line of myxofibrosarcoma [ Hum Cell, 2021, 34(6):1911-1918] | PubMed: 34383271 |
| Establishment and characterization of the NCC-GCTB4-C1 cell line: a novel patient-derived cell line from giant cell tumor of bone [ Hum Cell, 2021, 10.1007/s13577-021-00639-4] | PubMed: 34731453 |
| Establishment and characterization of novel patient-derived cell lines from giant cell tumor of bone [ Hum Cell, 2021, 10.1007/s13577-021-00579-z] | PubMed: 34304386 |
| The Meningioma Enhancer Landscape Delineates Novel Subgroups and Drives Druggable Dependencies [ Cancer Discov, 2020, CD-20-0160] | PubMed: 32703768 |
| Establishment and characterization of NCC-MFS2-C1: a novel patient-derived cancer cell line of myxofibrosarcoma [ Hum Cell, 2020, 10.1007/s13577-020-00420-z] | PubMed: 32870449 |
| Multi-omic Profiling Reveals Dynamics of the Phased Progression of Pluripotency. [ Cell Syst, 2019, 8(5):427-445] | PubMed: 31078527 |
| Intratumoural Heterogeneity Underlies Distinct Therapy Responses and Treatment Resistance in Glioblastoma. [ Cancers (Basel), 2019, 11(2)] | PubMed: 30736342 |
POLITICA DI RESO
La politica di reso incondizionato di Selleck Chemical garantisce ai nostri clienti unesperienza di acquisto online senza problemi. Se non sei in alcun modo soddisfatto del tuo acquisto, puoi restituire qualsiasi articolo entro 7 giorni dalla ricezione. In caso di problemi di qualità del prodotto, sia relativi al protocollo che al prodotto, puoi restituire qualsiasi articolo entro 365 giorni dalla data di acquisto originale. Si prega di seguire le istruzioni seguenti per la restituzione dei prodotti.
SPEDIZIONE E CONSERVAZIONE
I prodotti Selleck vengono trasportati a temperatura ambiente. Se ricevi il prodotto a temperatura ambiente, ti assicuriamo che il Dipartimento di Ispezione Qualità di Selleck ha condotto esperimenti per verificare che la conservazione a temperatura normale per un mese non influirà sullattività biologica dei prodotti in polvere. Dopo la raccolta, conservare il prodotto secondo le indicazioni descritte nella scheda tecnica. La maggior parte dei prodotti Selleck è stabile nelle condizioni raccomandate.
NON PER USO UMANO, DIAGNOSTICO VETERINARIO O TERAPEUTICO.
