Dati tecnici
| Formula | C14H19BCl2N2O4 |
||||||
| Peso molecolare | 361.03 | Numero CAS | 1072833-77-2 | ||||
| Solubilità (25°C)* | In vitro | DMSO | 72 mg/mL (199.42 mM) | ||||
| Ethanol | 72 mg/mL (199.42 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Aggiungere i solventi al prodotto singolarmente e in ordine.) |
|
||||||
|
* <1 mg/ml significa leggermente solubile o insolubile. * Si prega di notare che Selleck testa la solubilità di tutti i composti internamente e la solubilità effettiva può differire leggermente dai valori pubblicati. Ciò è normale ed è dovuto a leggere variazioni da lotto a lotto. * Spedizione a temperatura ambiente (I test di stabilità mostrano che questo prodotto può essere spedito senza alcuna misura di raffreddamento.) |
|||||||
Preparazione delle soluzioni stock
Attività biologica
| Descrizione | Ixazomib (MLN2238) inibisce il sito proteolitico (β5) simil-chimotripsina del 20S proteasome con IC50 e Ki di 3,4 nM e 0,93 nM in saggi acellulari, rispettivamente, e inibisce anche i siti proteolitici simil-caspasi (β1) e simil-tripsina (β2), con IC50 di 31 e 3500 nM. Ixazomib (MLN2238) induce l'autophagy. Fase 3. | ||||
|---|---|---|---|---|---|
| Target |
|
||||
| In vitro | A concentrazioni più elevate, questo composto inibisce anche i siti proteolitici caspasi-simili (β1) e tripsino-simili (β2) con IC50 di 31 nM e 3,5 uM, rispettivamente. Inibisce le cellule Calu-6 con una IC50 di 9,7 nM. MLN2238 è un inibitore selettivo, potente e reversibile del Proteasome nelle cellule tumorali. Questo composto mostra un'inibizione reversibile del Proteasome tempo-dipendente. Sia questo composto che Bortezomib mostrano un'inibizione reversibile del Proteasome tempo-dipendente; tuttavia, l'emivita di dissociazione del Proteasome per esso è determinata essere circa 6 volte più veloce di quella del Bortezomib (18 e 110 minuti, rispettivamente). Si dissocia più rapidamente dal Proteasome rispetto al Bortezomib, il che è coerente con un recupero più rapido dell'attività del Proteasome osservato nel saggio Proteasome-Glo. Ha un effetto farmacodinamico tumorale complessivo maggiore rispetto al Bortezomib, come valutato dall'inibizione del 20S. Questo composto è la forma biologicamente attiva di MLN9708. | ||||
| In vivo | MLN2238 induce una risposta farmacodinamica maggiore rispetto a Bortezomib nei tumori di xenotrapianto. Questo composto mostra una maggiore inibizione massima e sostenuta del Proteasome tumorale rispetto a Bortezomib nei modelli di xenotrapianto. Questi risultati confermano che la migliore esposizione tumorale osservata con questo agente si traduce in una migliore risposta farmacodinamica tumorale sia a livello che a valle del Proteasome. Mostra attività antitumorale nel modello di xenotrapianto CWR22. Questa sostanza chimica mostra risposte farmacodinamiche tumorali maggiori negli xenotrapianti WSU-DLCL2 rispetto a Bortezomib. Allo stesso modo, il trattamento con Bortezomib ha portato solo a un lieve aumento dei livelli di GADD34 nei tumori di xenotrapianto WSU-DLCL2, mentre esso ne induce fortemente l'espressione. Questo composto ha un profilo farmacodinamico e un'attività antitumorale migliorati rispetto a Bortezomib in entrambi i modelli OCI-Ly10 e PHTX22L. | ||||
| Caratteristiche | Un inibitore del Proteasome di prima classe che ha migliorato la farmacocinetica (PK), la farmacodinamica (PD) e l'attività antitumorale negli studi preclinici. |
Protocollo (da riferimento)
| Saggio della chinasi:[1] |
|
|---|---|
| Saggio cellulare:[1] |
|
| Studio sugli animali:[2] |
|
Riferimenti
|
Convalida del prodotto da parte del cliente
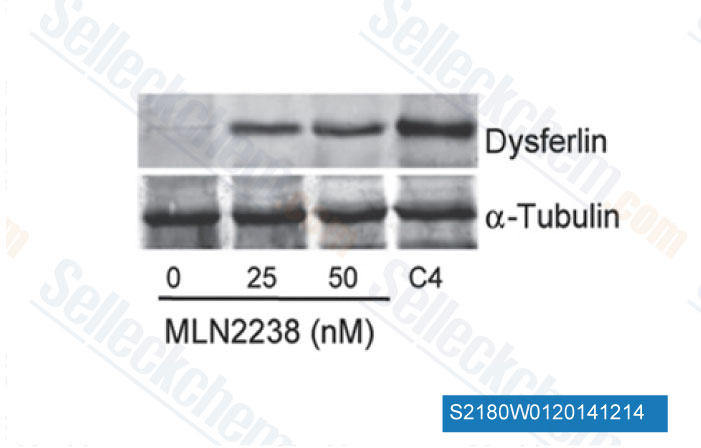
-
Dati da [ Sci Transl Med , 2014 , 6(250), 250ra112 ]
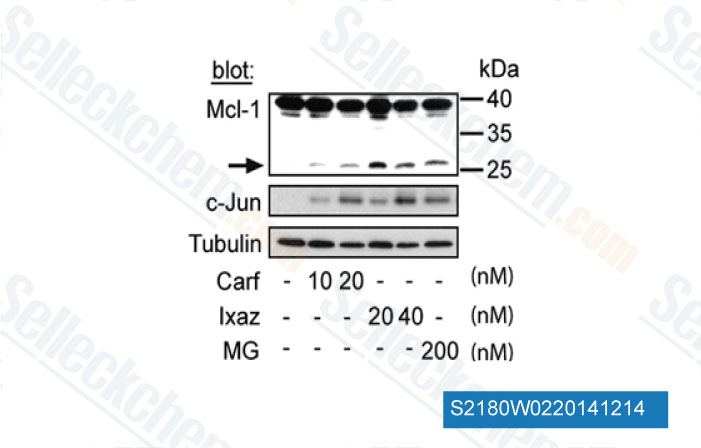
-
Dati da [ Cancer Lett , 2014 , 343(2), 286-94 ]
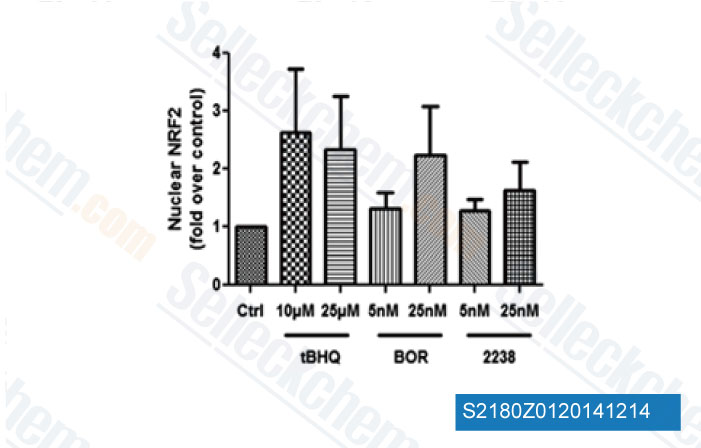
-
Dati da [ Hemoglobin , 2014 , 38(3), 188-95 ]
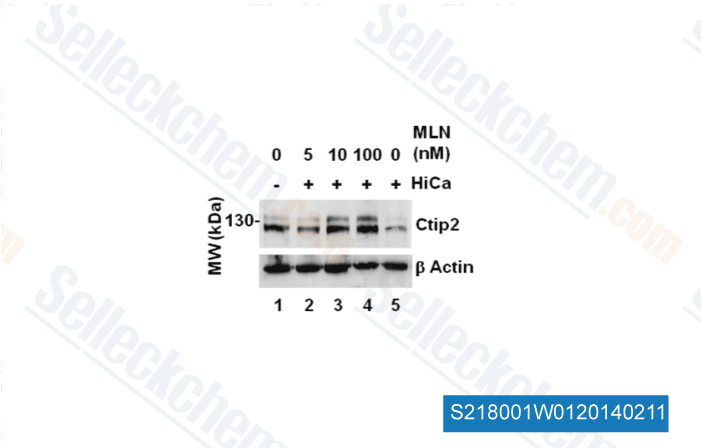
-
Dati da [ J Cell Sci , 2012 , 125(Pt 23), 5733-44 ]
Sellecks MLN2238 (Ixazomib) È stato citato da 71 Pubblicazioni
| Structural basis for allosteric modulation of M. tuberculosis proteasome core particle [ Nat Commun, 2025, 16(1):3138] | PubMed: 40169579 |
| A patient-derived T cell lymphoma biorepository uncovers pathogenetic mechanisms and host-related therapeutic vulnerabilities [ Cell Rep Med, 2025, S2666-3791(25)00102-8] | PubMed: 40147445 |
| Enhancing T cell cytotoxicity in multiple myeloma with bispecific αPD-L1 × αCD3 T cell engager-armed T cells and low-dose bortezomib therapy [ Biomed Pharmacother, 2025, 184:117878] | PubMed: 39891948 |
| High-Throughput Drug Screening of Clear Cell Ovarian Cancer Organoids Reveals Vulnerability to Proteasome Inhibitors and Dinaciclib and Identifies AGR2 as a Therapeutic Target [ Cancer Res Commun, 2025, 5(6):1018-1033] | PubMed: 40459063 |
| Integrated transcriptomics- and structure-based drug repositioning identifies drugs with proteasome inhibitor properties [ Sci Rep, 2024, 14(1):18772] | PubMed: 39138277 |
| A combinatorial therapeutic approach to enhance FLT3-ITD AML treatment [ Cell Rep Med, 2023, 10.1016/j.xcrm.2023.101286] | PubMed: 37951217 |
| Targeting ITGB4/SOX2-driven lung cancer stem cells using proteasome inhibitors [ iScience, 2023, 26(8):107302] | PubMed: 37554452 |
| Dual inhibition of HSF1 and DYRK2 impedes cancer progression [ Biosci Rep, 2023, 43(1)BSR20222102] | PubMed: 36622366 |
| Proteasome inhibition as a therapeutic target for the fungal pathogen Cryptococcus neoformans [ Microbiol Spectr, 2023, 11(5):e0190423] | PubMed: 37750732 |
| Proteasome inhibition as a therapeutic target for the fungal pathogen Cryptococcus neoformans [ Microbiol Spectr, 2023, 10.1128/spectrum.01904-23] | PubMed: 37750732 |
POLITICA DI RESO
La politica di reso incondizionato di Selleck Chemical garantisce ai nostri clienti unesperienza di acquisto online senza problemi. Se non sei in alcun modo soddisfatto del tuo acquisto, puoi restituire qualsiasi articolo entro 7 giorni dalla ricezione. In caso di problemi di qualità del prodotto, sia relativi al protocollo che al prodotto, puoi restituire qualsiasi articolo entro 365 giorni dalla data di acquisto originale. Si prega di seguire le istruzioni seguenti per la restituzione dei prodotti.
SPEDIZIONE E CONSERVAZIONE
I prodotti Selleck vengono trasportati a temperatura ambiente. Se ricevi il prodotto a temperatura ambiente, ti assicuriamo che il Dipartimento di Ispezione Qualità di Selleck ha condotto esperimenti per verificare che la conservazione a temperatura normale per un mese non influirà sullattività biologica dei prodotti in polvere. Dopo la raccolta, conservare il prodotto secondo le indicazioni descritte nella scheda tecnica. La maggior parte dei prodotti Selleck è stabile nelle condizioni raccomandate.
NON PER USO UMANO, DIAGNOSTICO VETERINARIO O TERAPEUTICO.
