Dati tecnici
| Formula | C20H20N4O |
||||||||||
| Peso molecolare | 332.4 | Numero CAS | 1000669-72-6 | ||||||||
| Solubilità (25°C)* | In vitro | DMSO | 67 mg/mL (201.56 mM) | ||||||||
| Ethanol | 67 mg/mL (201.56 mM) | ||||||||||
| Water | Insoluble | ||||||||||
| In vivo (Aggiungere i solventi al prodotto singolarmente e in ordine.) |
|
||||||||||
|
* <1 mg/ml significa leggermente solubile o insolubile. * Si prega di notare che Selleck testa la solubilità di tutti i composti internamente e la solubilità effettiva può differire leggermente dai valori pubblicati. Ciò è normale ed è dovuto a leggere variazioni da lotto a lotto. * Spedizione a temperatura ambiente (I test di stabilità mostrano che questo prodotto può essere spedito senza alcuna misura di raffreddamento.) |
|||||||||||
Preparazione delle soluzioni stock
Attività biologica
| Descrizione | KW-2449 è un inibitore multi-target, principalmente per Flt3 con un IC50 di 6,6 nM, moderatamente potente per FGFR1, Bcr-Abl e Aurora A; scarso effetto su PDGFRβ, IGF-1R, EGFR. Fase 1. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Target |
|
|||||||||||
| In vitro | KW-2449, un inibitore multichinasico di FLT3, ABL, ABL-T315I e Aurora kinase, è sotto indagine per il trattamento di pazienti affetti da leucemia. Questo composto mostra potenti effetti inibitori della crescita sulle cellule leucemiche con mutazioni FLT3 mediante l'inibizione della FLT3 chinasi, con conseguente down-regulation di FLT3/STAT5 fosforilato, arresto in G1 e apoptosi. La somministrazione orale di questa sostanza chimica mostra un'inibizione dose-dipendente e significativa della crescita tumorale nel modello di xenotrapianto con mutazione FLT3 con minima soppressione del midollo osseo. Nella leucemia umana con FLT3 wild-type, induce la riduzione dell'istone H3 fosforilato, l'arresto in G2/M e l'apoptosi. Nella leucemia resistente all'Imatinib, questo agente contribuisce a superare la resistenza mediante la simultanea down-regulation di BCR/ABL e Aurora kinases. L'attività inibitoria di questo composto non è influenzata dalla presenza di proteine plasmatiche umane, come l'α1-glicoproteina acida. Possiede una potente attività inibitoria della crescita contro vari tipi di leucemia tramite diversi meccanismi d'azione. Questo inibitore ha un'attività significativa e giustifica uno studio clinico in pazienti affetti da leucemia con mutazioni FLT3 e mutazioni resistenti all'Imatinib. I livelli di fosforilazione di FLT3 e STAT5 sono diminuiti da questa sostanza chimica in modo dose-dipendente. Inoltre, inibisce potentemente ABL-T315I, che è associato alla resistenza all'IM, con un IC50 di 4 nM. D'altra parte, questo composto ha scarso effetto su PDGFRβ, IGF-1R, EGFR e varie serina/treonina chinasi anche a una concentrazione di 1 μM. Ha potenti attività inibitorie della crescita non solo contro le cellule leucemiche che esprimono FLT3/ITD, ma anche contro le cellule leucemiche attivate da FLT3/KDM e le cellule leucemiche che sovraesprimono FLT3 wild-type. In accordo con l'effetto inibitorio della crescita, questo agente sopprime le fosforilazioni di FLT3 (P-FLT3) e della sua molecola a valle fosfo-STAT5 (P-STAT5) nelle cellule MOLM-13 in modo dose-dipendente. Inoltre, aumenta la percentuale di cellule in fase G1 del ciclo cellulare e riduce reciprocamente la percentuale di cellule in fase S, con conseguente aumento della popolazione di cellule apoptotiche. Questo composto può defosforilare la chinasi WT-FLT3 costitutivamente attiva, ma non inibisce la proliferazione delle cellule leucemiche se non sono principalmente dipendenti dalla chinasi FLT3. Viene rapidamente assorbito e convertito in un metabolita principale M1. Studi preclinici rivelano che questa sostanza chimica viene convertita dalla monoaminossidasi-B (MAO-B) e dall'aldeide ossidasi nel suo metabolita principale M1. Questo agente media la citotossicità tramite l'inibizione di FLT3/ITD. È un inibitore diretto di FLT3 e induce l'inibizione del suo bersaglio a valle STAT5. Questo composto interagisce sinergicamente con gli HDACI per indurre apoptosi nelle cellule CML Ph+ in modo tempo- e concentrazione-dipendente. Migliora sinergicamente la letalità di vorinostat/SNDX275 nelle cellule CML. Questi regimi di inibitori sono attivi contro ulteriori cellule leucemiche Bcr/Abl+ resistenti all'IM. Riduce moderatamente la fosforilazione dell'istone H3, un indicatore dell'attività di Aurora B, nelle cellule K562 trattate con nocodazolo. | |||||||||||
| In vivo | Nel modello di xenotrapianto tumorale MOLM-13, la somministrazione orale di KW-2449 per 14 giorni mostra un potente e significativo effetto antitumorale in modo dose-dipendente. | |||||||||||
| Caratteristiche | Studiato come FLT3 inhibitor in studi clinici, con altri in fase di sviluppo precoce. |
Protocollo (da riferimento)
| Saggio della chinasi:[2] |
|
|---|---|
| Saggio cellulare: [1] |
|
| Studio sugli animali:[3] |
|
Riferimenti
|
Convalida del prodotto da parte del cliente
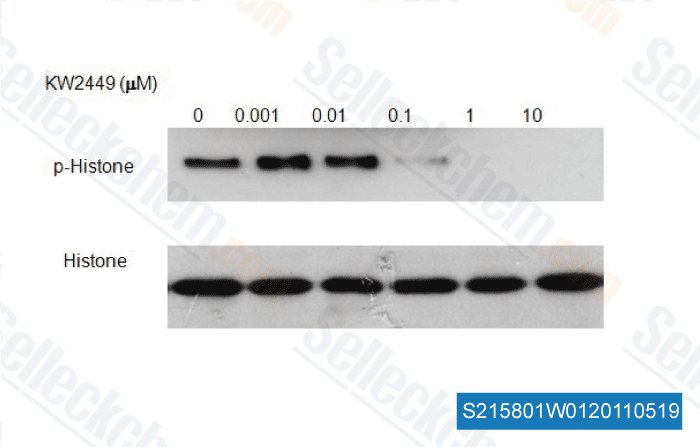
-
, , Dr. Zhang of Tianjin Medical University
Sellecks KW-2449 È stato citato da 12 Pubblicazioni
| Integrative analysis of drug response and clinical outcome in acute myeloid leukemia [ Cancer Cell, 2022, S1535-6108(22)00312-9] | PubMed: 35868306 |
| A community challenge for a pancancer drug mechanism of action inference from perturbational profile data [ Cell Rep Med, 2022, 3(1):100492] | PubMed: 35106508 |
| Phosphorylation of SHP2 at Tyr62 Enables Acquired Resistance to SHP2 Allosteric Inhibitors in FLT3-ITD-Driven AML [ Cancer Res, 2022, 82(11):2141-2155] | PubMed: 35311954 |
| KW-2449 and VPA exert therapeutic effects on human neurons and cerebral organoids derived from MECP2-null hESCs [ Stem Cell Res Ther, 2022, 13(1):534] | PubMed: 36575558 |
| Evaluation of CML TKI Induced Cardiovascular Toxicity and Development of Potential Rescue Strategies in a Zebrafish Model [ Front Pharmacol, 2021, 12:740529] | PubMed: 34733159 |
| Mechanisms of Oncogenesis in the Primary Liver Cell Cancer [ DTIC, 2021, 53] | PubMed: None |
| The Global Phosphorylation Landscape of SARS-CoV-2 Infection [ Cell, 2020, 182(3):685-712.e19] | PubMed: 32645325 |
| Synergistic Anti Leukemia Effect of a Novel Hsp90 and a Pan Cyclin Dependent Kinase Inhibitors. [ Molecules, 2020, 8;25(9) pii: E2220] | PubMed: 32397330 |
| Small-Molecule and CRISPR Screening Converge to Reveal Receptor Tyrosine Kinase Dependencies in Pediatric Rhabdoid Tumors. [ Cell Rep, 2019, 28(9):2331-2344] | PubMed: 31461650 |
| Drug Target Commons: A Community Effort to Build a Consensus Knowledge Base for Drug-Target Interactions [Tang J Cell Chem Biol, 2018, 25(2):224-229] | PubMed: 29276046 |
POLITICA DI RESO
La politica di reso incondizionato di Selleck Chemical garantisce ai nostri clienti unesperienza di acquisto online senza problemi. Se non sei in alcun modo soddisfatto del tuo acquisto, puoi restituire qualsiasi articolo entro 7 giorni dalla ricezione. In caso di problemi di qualità del prodotto, sia relativi al protocollo che al prodotto, puoi restituire qualsiasi articolo entro 365 giorni dalla data di acquisto originale. Si prega di seguire le istruzioni seguenti per la restituzione dei prodotti.
SPEDIZIONE E CONSERVAZIONE
I prodotti Selleck vengono trasportati a temperatura ambiente. Se ricevi il prodotto a temperatura ambiente, ti assicuriamo che il Dipartimento di Ispezione Qualità di Selleck ha condotto esperimenti per verificare che la conservazione a temperatura normale per un mese non influirà sullattività biologica dei prodotti in polvere. Dopo la raccolta, conservare il prodotto secondo le indicazioni descritte nella scheda tecnica. La maggior parte dei prodotti Selleck è stabile nelle condizioni raccomandate.
NON PER USO UMANO, DIAGNOSTICO VETERINARIO O TERAPEUTICO.
