Dati tecnici
| Formula | C25H26ClN5O3 |
||||||
| Peso molecolare | 479.96 | Numero CAS | 468740-43-4 | ||||
| Solubilità (25°C)* | In vitro | DMSO | 96 mg/mL (200.01 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Aggiungere i solventi al prodotto singolarmente e in ordine.) |
|
||||||
|
* <1 mg/ml significa leggermente solubile o insolubile. * Si prega di notare che Selleck testa la solubilità di tutti i composti internamente e la solubilità effettiva può differire leggermente dai valori pubblicati. Ciò è normale ed è dovuto a leggere variazioni da lotto a lotto. * Spedizione a temperatura ambiente (I test di stabilità mostrano che questo prodotto può essere spedito senza alcuna misura di raffreddamento.) |
|||||||
Preparazione delle soluzioni stock
Attività biologica
| Descrizione | BMS-536924 (CS-0117) è un inibitore di IGF-1R/IR competitivo per l'ATP con IC50 di 100 nM/73 nM, modesta attività per Mek, Fak e Lck con pochissima attività per Akt1, MAPK1/2. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Target |
|
|||||||||||
| In vitro | BMS-536924 inibisce anche FAK e Lck con IC50 di 150 nM e 341 nM, rispettivamente. Questo composto inibisce la proliferazione cellulare e altera la fosforilazione di Akt e MAPK. Inibisce la segnalazione di IGF-1R stimolata da IGF-I nelle cellule MCF10A e blocca l'attività costitutiva di IGF-1R nelle cellule CD8-IGF-1R-MCF10A. La preincubazione delle cellule MCF10A con 1 μM di questo composto chimico blocca completamente la capacità di IGF-I di stimolare la fosforilazione di IGF-1R. La stimolazione di IGF-I porta a un aumento della fosforilazione di ERK1/2, GSK3β e Akt. Questo composto inibisce questa fosforilazione indotta da ligando. Il trattamento delle cellule CD8-IGF-1R-MCF10A con questo inibitore provoca un'inibizione dose-dipendente della fosforilazione con inibizione parziale a 0,01 μM e 0,1 μM, ma un'inibizione completa del recettore a una concentrazione di 1 μM. L'inibizione massima di IGF-1R fosforilato si osserva già dopo 10 minuti di incubazione. Mantiene la sua capacità di inibire la fosforilazione di IGF-1R fino a 48 ore. L'aggiunta di questo agente inibisce la fosforilazione di Akt in modo tempo-dipendente a partire da 1 ora. Entro 48 ore, l'attivazione di Akt è completamente bloccata. Il trattamento con questo composto mostra attività antiproliferativa in un pannello di linee cellulari tumorali, incluse le cellule TC32, HT1080/S, SK-LMS-1, H513 e CTR. pIGF-1R/pIR è attivato dalla stimolazione con IGF-I/insulina e l'attivazione è inibita da questo composto chimico con potenze simili nelle linee cellulari Rh41 e Rh36. L'espressione della morte cellulare programmata 4 (PDCD4), il clivaggio della poli(ADP-ribosio) polimerasi (PARP) e della caspasi-3 sono regolati positivamente nelle cellule Rh41 trattate con questo inibitore. | |||||||||||
| In vivo | La somministrazione orale di BMS-536924 a 100-300 mpk inibisce fortemente il modello tumorale IGR-1R Sal. L'efficacia è osservata anche nel modello di carcinoma del colon umano Colo205 non ingegnerizzato. La somministrazione orale di questo composto con una programmazione una volta al giorno (100-300 mpk) o due volte al giorno (50, 100 mpk) dimostra attività antitumorale in questo modello tumorale. Il test di tolleranza al glucosio orale (OGTT) mostra che 100 mpk (b.i.d.) causa un'elevazione significativa dei livelli di glucosio dopo la sfida con glucosio. I parametri farmacocinetici di questo composto chimico, somministrato oralmente in poli(etilenglicole) 400 e acqua (80:20 v/v), sono determinati in topo, ratto, cane e scimmia. Una buona biodisponibilità è evidente in tutte le specie. Una significativa farmacocinetica non lineare è osservata nei roditori a dosi p.o. crescenti. Questo composto riduce il volume dei trapianti tumorali di cellule CD8-IGF-1R-MCF10A dopo due settimane di trattamento (100 mg/kg) al 76%. La somministrazione orale di 70 mg/kg di questo composto chimico inibisce significativamente la crescita tumorale (cellule TGBC-1TKB) inoculate in topi nudi. Regola positivamente l'apoptosi nei tumori di trapianti. Il trattamento non ha effetti avversi sul peso corporeo dei topi o sui livelli di glucosio al momento della morte, suggerendo una tossicità tollerabile. |
Protocollo (da riferimento)
| Saggio della chinasi: |
|
|---|---|
| Saggio cellulare: |
|
| Studio sugli animali: |
|
Riferimenti
|
Convalida del prodotto da parte del cliente
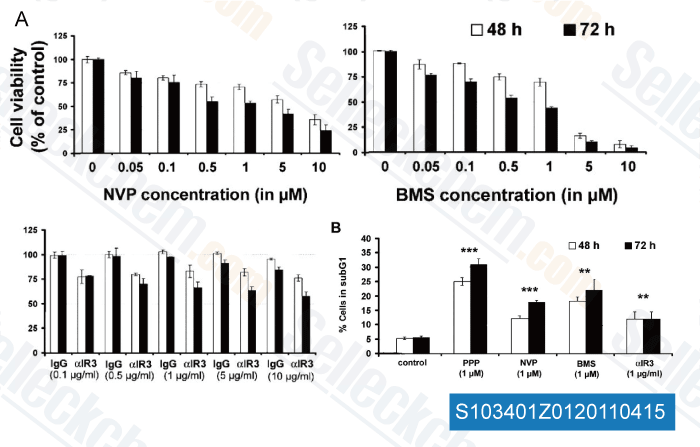
-
Dati da [ Clin Cancer Res , 2011 , 17, 2237-2249 ]
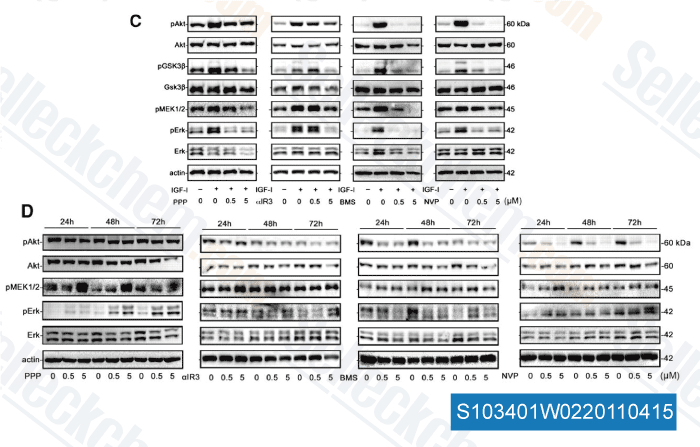
-
Dati da [ Clin Cancer Res , 2011 , 17, 2237-2249 ]
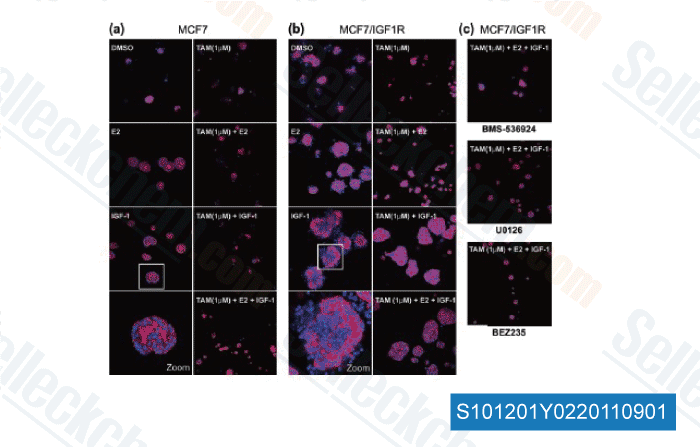
-
Dati da [ Breast Cancer Res , 2011 , 13, R52 ]
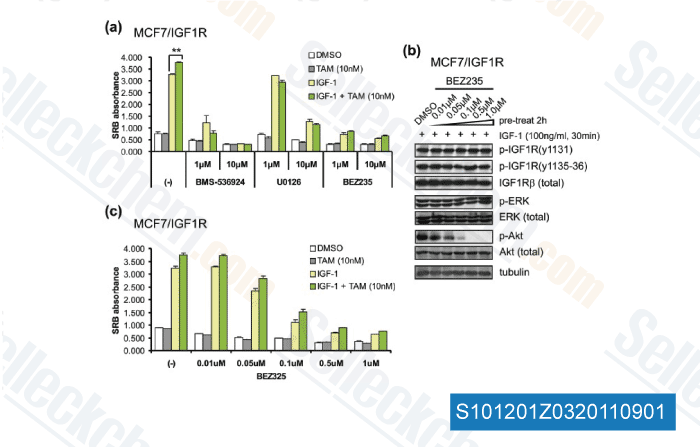
-
Dati da [ Breast Cancer Res , 2011 , 13, R52 ]
Sellecks BMS-536924 È stato citato da 27 Pubblicazioni
| Haploinsufficiency of miR-143 and miR-145 reveal targetable dependencies in resistant del(5q) myelodysplastic neoplasm [ Leukemia, 2025, 39(4):917-928] | PubMed: 40000845 |
| Inhibition of Selenoprotein I promotes ferroptosis and reverses resistance to platinum chemotherapy by impairing Akt phosphorylation in ovarian cancer [ MedComm (2020), 2024, 5(12):e70033] | PubMed: 39669976 |
| High-Content and High-Throughput Clonogenic Survival Assay Using Fluorescence Barcoding [ Cancers -Basel), 2023, 15(19)4772] | PubMed: 37835466 |
| SFRP4+ stromal cell subpopulation with IGF1 signaling in human endometrial regeneration [ Cell Discov, 2022, 8(1):95] | PubMed: 36163341 |
| Multi-omics characterization of autophagy-related molecular features for therapeutic targeting of autophagy [ Nat Commun, 2022, 13(1):6345] | PubMed: 36289218 |
| FER-mediated phosphorylation and PIK3R2 recruitment on IRS4 promotes AKT activation and tumorigenesis in ovarian cancer cells [ Elife, 2022, 11e76183] | PubMed: 35550247 |
| Exosomes from cisplatin-induced dormant cancer cells facilitate the formation of premetastatic niche in bone marrow through activating glycolysis of BMSCs [ Front Oncol, 2022, 12:922465] | PubMed: 36568212 |
| Intermittent parathyroid hormone improves orthodontic retention via insulin-like growth factor-1 [ Oral Dis, 2021, 27(2):290-300] | PubMed: 32608117 |
| Manganese Acts upon Insulin/IGF Receptors to Phosphorylate AKT and Increase Glucose Uptake in Huntington's Disease Cells [ Mol Neurobiol, 2020, 57(3):1570-1593] | PubMed: 31797328 |
| Loss of N-Glycanase 1 Alters Transcriptional and Translational Regulation in K562 Cell Lines [ G3 (Bethesda), 2020, 4;10(5):1585-1597] | PubMed: 32265286 |
POLITICA DI RESO
La politica di reso incondizionato di Selleck Chemical garantisce ai nostri clienti unesperienza di acquisto online senza problemi. Se non sei in alcun modo soddisfatto del tuo acquisto, puoi restituire qualsiasi articolo entro 7 giorni dalla ricezione. In caso di problemi di qualità del prodotto, sia relativi al protocollo che al prodotto, puoi restituire qualsiasi articolo entro 365 giorni dalla data di acquisto originale. Si prega di seguire le istruzioni seguenti per la restituzione dei prodotti.
SPEDIZIONE E CONSERVAZIONE
I prodotti Selleck vengono trasportati a temperatura ambiente. Se ricevi il prodotto a temperatura ambiente, ti assicuriamo che il Dipartimento di Ispezione Qualità di Selleck ha condotto esperimenti per verificare che la conservazione a temperatura normale per un mese non influirà sullattività biologica dei prodotti in polvere. Dopo la raccolta, conservare il prodotto secondo le indicazioni descritte nella scheda tecnica. La maggior parte dei prodotti Selleck è stabile nelle condizioni raccomandate.
NON PER USO UMANO, DIAGNOSTICO VETERINARIO O TERAPEUTICO.
