uitsluitend voor onderzoeksdoeleinden
Zidovudine Reverse Transcriptase remmer
Cat.Nr.S2579
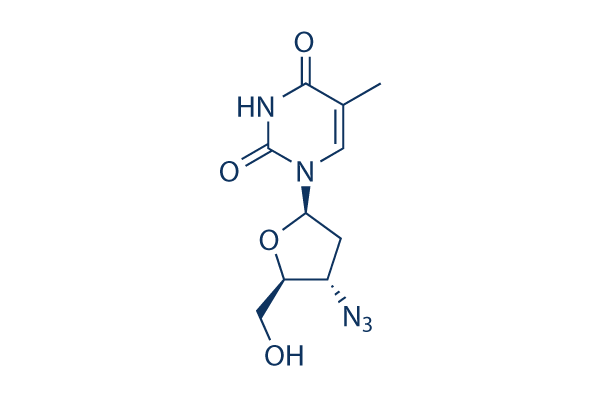
Chemische structuur
Moleculair gewicht: 267.24
Kwaliteitscontrole
| Gerelateerde doelwitten | Integrase Bacterial Antibiotics Anti-infection Fungal Antiviral COVID-19 Parasite HIV HCV Protease |
|---|---|
| Overige Reverse Transcriptase Inhibitoren | Dapivirine (TMC120) Fangchinoline Salicylanilide 3'-Fluoro-3'-deoxythymidine (Alovudine) Ulonivirine Lersivirine (UK-453061) Bifendate 4-Chloro-2-(trifluoroacetyl)aniline hydrochloride |
Celkweek, behandeling & werkconcentratie
| Cellijnen | Assaytype | Concentratie | Incubatietijd | Formulering | Activiteitsbeschrijving | PMID |
|---|---|---|---|---|---|---|
| human C8166 cells | Function assay | Antiviral activity against Human immunodeficiency virus 1 infected in human C8166 cells assessed as inhibition of virus-induced cytopathic effect, EC50=4e-06 μM | ||||
| PBMC | Function assay | 1 μM | Antiviral activity against HIV1 TEKI replication in PBMC at 1 uM, IC50=0.00014 μM | |||
| human H9 cells | Function assay | 6 days | Antiviral activity against Human immunodeficiency virus 1 3B infected in human H9 cells infected with 6.25 uL of virus stock assessed as expression of p24 antigen after 6 days postinfection by ELISA, IC50=0.3 nM | |||
| AA5 cells | Function assay | Antiviral activity against of Human immunodeficiency virus 1 3B infected in AA5 cells infected with 1.56 uL of virus stock assessed as inhibition of viral Reverse transcriptase by [3H]TTP incorporation assay, IC50=0.3 nM | ||||
| CEM cells | Function assay | Concentration of the drug resulting in 50% reduction of the viral cytopathic effect against HIV-1 replication in CEM cells, EC50=0.32 nM | ||||
| MT4 cells | Function assay | 4 days | Antiviral activity against HIV1 3B assessed as inhibition of virus-induced cytopathogenicity in MT4 cells after 4 days by MTT assay, EC50=0.7 nM | |||
| human MT2 cells | Function assay | 1 h | Antiviral activity against HIV1 subtype B-3B infected in 1 hr-pretreated human MT2 cells assessed as inhibition of multicycle replication measured on day 5 postinfection by RT SPA, EC50=1.2 nM | |||
| C8166 cells | Function assay | Inhibition of HIV1-3B replication in C8166 cells, EC50=1.9 nM | ||||
| CEM-SS cell | Function assay | Inhibitory activity against the HIV-1-induced cytopathic effect in CEM-SS cell line, IC50=0.002 μM | ||||
| PBLs | Function assay | Antiviral activity against subtype isolate G strain in PBLs (peripheral blood lymphocytes), IC50=0.002 μM | ||||
| human lymphocyte CEM/0 cell line | Function assay | Anti HIV-1 activity in human lymphocyte CEM/0 cell line, EC50=0.003 μM | ||||
| Jurkat cell | Function assay | Inhibitory concentration against HIV-1 infected Jurkat cell lines, IC50=0.01 μM | ||||
| human H9 cells | Cytotoxicity assay | 6 days | Cytotoxicity against human H9 cells after 6 days by MTT assay, EC50=0.01 μM | |||
| C3H/3T3 cells | Function assay | Concentration of compound required to inhibit HIV-1 induced cytopathogenicity of MSV-induced transformation of C3H/3T3 cells by 50%, EC50=0.02 μM | ||||
| U937 cells | Function assay | Effective concentration required for antiviral activity against Macrophage cell line of U937 cells of Human by XTT assay, EC50=0.03 μM | ||||
| Klik om meer experimentele gegevens over de cellijn te bekijken | ||||||
Chemische informatie, Opslag en Stabiliteit
| Moleculair gewicht | 267.24 | Formule | C10H13N5O4 |
Opslag (Vanaf de ontvangstdatum) | |
|---|---|---|---|---|---|
| CAS-nr. | 30516-87-1 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | Azidothymidine, NSC 602670 | Smiles | CC1=CN(C(=O)NC1=O)C2CC(C(O2)CO)N=[N+]=[N-] | ||
Oplosbaarheid
|
In vitro |
DMSO
: 53 mg/mL
(198.32 mM)
Ethanol : 53 mg/mL Water : 26 mg/mL |
Molariteitscalculator
|
In vivo |
|||||
In vivo Formuleringscalculator (Heldere oplossing)
Stap 1: Voer de onderstaande informatie in (Aanbevolen: Een extra dier voor het geval van verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in het gedeelte Oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-mastervloeistof: mg geneesmiddel vooraf opgelost in μL DMSO ( Concentratie mastervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de partij geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toeμL PEG300, mengen en helder maken, voeg vervolgens toeμL Tween 80, mengen en helder maken, voeg vervolgens toe μL ddH2O, mengen en helder maken.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toe μL Maïsolie, mengen en helder maken.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysische methoden zoals vortexen, echografie of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
Reverse transcriptase
|
|---|---|
| In vitro |
Zidovudine-voorbehandeling heeft een krachtige anti-HIV-1-activiteit in de nieuw geïnfecteerde T- en monocytaire cellen, maar niet in chronisch geïnfecteerde cellen. Remming van de reverse transcriptie door deze verbinding vermindert de p24-antigeeniveaus bescheiden, verminderde HIV-1 gag met 19-voudig, en remt de detectie van 2-LTR HIV-1-DNA. Deze verbinding en dideoxynucleosiden putten de wild-type mitochondriale DNA-niveaus uit en verhogen de gedeleteerde mitochondriale DNA-niveaus in gekweekte Kearns-Sayre-syndroomfibroblasten. Deze chemische stof (AZT, 0,1-50 mM) heeft een concentratieafhankelijk onderdrukkend effect op de groei van granulocyt-monocyt kolonie vormende eenheid (CFU-GM) afgeleide kolonies. Blootstelling aan deze verbinding induceert ook een concentratieafhankelijk onderdrukkend effect (35-90%) op de genexpressie van de GM-CSF-receptor type alfa (GM-CSFR alfa). Het veroorzaakt een veel lagere afname (15-22%) op het IL-3-receptor type alfa (IL-3R alfa) boodschapperniveau, en heeft een onbeduidend effect op de glyceraldehyde 3-fosfaatdehydrogenase (GAPDH) en c-myc boodschapperniveaus. Deze chemische stof veroorzaakt een concentratieafhankelijke remming van de niveaus van het mRNA van Epo-receptoren en c-fos, terwijl het niveau van c-myc mRNA onaangetast blijft. Het remt ook de proteïnekinase C (PKC) activiteit op een concentratie- en tijdsafhankelijke manier, waardoor 50% remming optreedt bij 10 mM binnen 3 uur. De door deze verbinding geïnduceerde down-regulatie van Epo-receptoren en c-fos expressie gekoppeld aan remming van Epo-receptor-gemedieerde signaaltransductie via PKC zijn belangrijke bijdragende factoren aan AZT-geïnduceerde erytroïde toxiciteit. Deze verbinding zou de HDR-efficiëntie kunnen verminderen. Het vermindert CRISPR-gemedieerde sequentie-specifieke genoom knock-in-gebeurtenissen terwijl het de knock-out-efficiëntie verhoogt . |
Referenties |
|
Informatie klinische proef
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Rekrutering | Aandoeningen | Sponsor/Medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT03991013 | Completed | HIV Infections |
University of Cape Town|Wellcome Trust|Médecins Sans Frontières Belgium |
August 8 2019 | Phase 2 |
| NCT03642704 | Completed | Mother to Child HIV Transmission |
ANRS Emerging Infectious Diseases |
February 22 2017 | Phase 4 |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, kunt u een bericht achterlaten.
Veelgestelde vragen
Vraag 1:
Do you happen to have any information regarding its half-life?
Antwoord:
Its half-life in human is available (http://www.rxlist.com/retrovir-drug/clinical-pharmacology.htm), about 0.5-3 hours in adult subjects.
